监管事务外包市场
监管事务外包市场规模、份额、增长和行业分析,按服务(监管咨询、法律代表、提交准备和管理、质量和合规性等)、按应用、按最终用户(制药和生物技术公司、医疗器械制造商)以及区域分析, 2024-2031
页面: 190 | 基准年: 2023 | 发布: 2025年1月 | 作者: Sunanda G. | 最近更新: 2026年3月
立即咨询
页面: 190 | 基准年: 2023 | 发布: 2025年1月 | 作者: Sunanda G. | 最近更新: 2026年3月
监管事务外包是指将监管合规任务委托给第三方服务提供商的做法,常见于制药、生物技术、医疗器械和医疗保健等行业。
这种方法涉及管理监管策略的制定、文件准备、提交产品批准申请、合规性监控和上市后监督。它使组织能够专注于研发等核心活动,同时确保有效地满足全球不同市场的合规性。
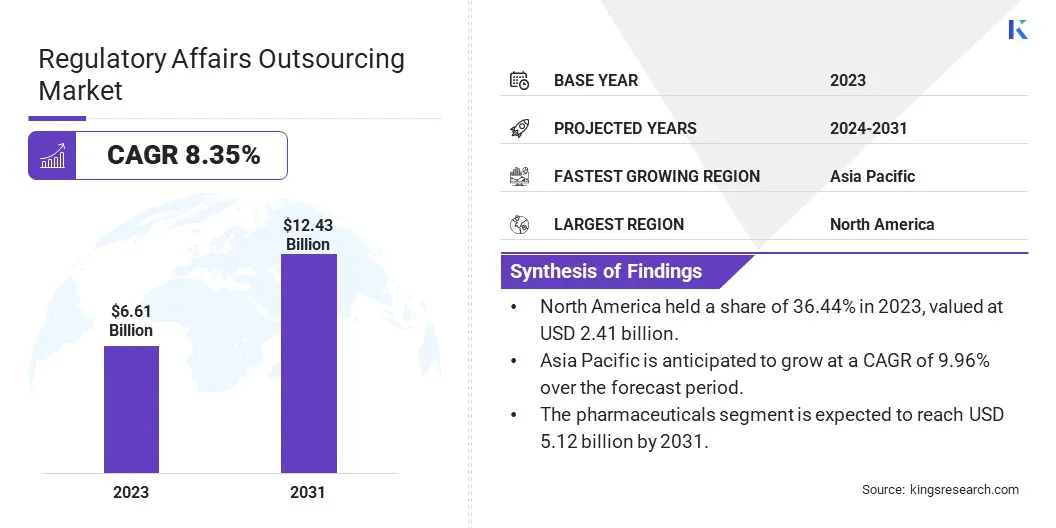
2023年,全球监管事务外包市场规模为66.1亿美元,预计将从2024年的70.9亿美元增长到2031年的124.3亿美元,预测期内复合年增长率为8.35%。
在全球监管框架日益复杂以及对具有成本效益的合规解决方案不断增长的需求的推动下,该市场正在经历显着增长。此外,临床试验的扩大、先进治疗药品的兴起以及对上市后监测的日益关注进一步推动了市场的扩张。
全球监管事务外包市场的主要公司有Accell Clinical Research, LLC、Genpact、WuXi AppTec、Medpace、Charles River Laboratories、CRITERIUM, INC.、iuvo BioScience, llc.、Covance、Freyr、ICON plc、PHARMALEX GMBH.、Groupe ProductLife S.A.、Parexel International (MA) Corporation、Biomapas Group、Thermo Fisher Scientific Inc. (PPD)、和其他人。
外包监管事务职能有助于提高对质量和合规性的关注,从而推动市场的增长。监管机构越来越重视安全和质量标准,特别是在医疗保健和制药等监管严格的行业。
市场驱动力
“全球临床试验数量不断增加”
全球临床试验数量的不断增加正在推动监管事务外包市场的增长。随着对创新和新疗法开发的日益关注,全球进行的临床试验数量有所增加。
管理这些试验的监管方面,包括获得批准、确保遵守当地法规以及提交所需文件,是复杂且耗时的。
外包合作伙伴凭借其在全球监管要求方面的专业知识,帮助简化审批流程、减少延误,并确保临床试验按照必要的监管标准进行。临床试验中对监管支持的需求不断增加,进一步推动了市场的扩张。
市场挑战
“解决多个地区的监管合规问题”
限制监管事务外包市场增长的一个重要因素是保持遵守多个地区不同监管要求的挑战。全球市场在法规、文件标准和审批时间表方面存在显着差异,给外包服务提供商带来了复杂性。
这种可变性增加了延迟、错误和潜在不合规的风险,影响了外包运营的效率和有效性。
为了应对这一挑战,企业越来越多地采用先进的数字工具和人工智能(AI)简化监管流程并确保文件的准确性。利用人工智能驱动的平台提供实时更新和预测分析,帮助提供商适应不断变化的法规。
此外,公司还通过建立本地团队或与市场专家建立合作伙伴关系来投资特定地区的专业知识,以更有效地应对监管环境。这些方法增强了适应性,最大限度地降低了合规风险,并改善了服务交付,从而减轻了监管复杂性对市场增长的影响。
市场趋势
“监管外包随着数字健康趋势而兴起”
移动健康应用程序、可穿戴设备和远程医疗解决方案等数字健康产品和服务的快速扩张正在促进监管事务外包市场的增长。监管机构正在制定新的框架,以应对数字健康创新带来的独特挑战。
这些产品通常需要采用不同的方法来实现监管合规,包括数据隐私问题、网络安全标准和新颖的临床试验要求。
开发数字健康解决方案的公司正在转向拥有该领域专业知识的外包公司,以应对不断变化的法规
| 分割 | 细节 |
| 按服务 | 监管咨询、法律代表、提交准备和管理、质量与合规性、其他 |
| 按申请 | 药品、医疗器械、生物制品、其他 |
| 按最终用户 | 制药和生物技术公司、医疗器械制造商、合同研究组织 (CRO) |
| 按地区 | 北美:美国、加拿大、墨西哥 |
| 欧洲:法国、英国、西班牙、德国、意大利、俄罗斯、欧洲其他国家/地区 | |
| 亚太:中国、日本、印度、澳大利亚、东盟、韩国、亚太其他地区 | |
| 中东和非洲:土耳其、阿联酋、沙特阿拉伯、南非、中东和非洲其他地区 | |
| 南美洲:巴西、阿根廷、南美洲其他地区 |
按地区划分,全球市场分为北美、欧洲、亚太地区、中东和非洲以及拉丁美洲。

2023年,北美监管事务外包市场占据约36.44%的份额,价值24.1亿美元。该地区成熟的制药和生物技术产业正在推动这一扩张。药品审批量不断增加,临床试验,治疗方法的持续创新需要专家监管服务来应对复杂的审批流程。
随着公司寻求满足严格的监管要求(例如 FDA 的要求),同时加快产品开发时间,对专业监管事务外包的需求不断增加
预计亚太地区在预测期内将以 9.96% 的复合年增长率增长最快。在研发投资增加、生物制药进步以及医疗保健市场不断扩大的推动下,亚太地区的制药和生物技术行业正在经历快速增长。
随着该地区生物技术和制药公司数量的不断增加,对监管专业知识的需求也不断增长。
外包监管事务使这些公司能够管理当地和国际监管的复杂性,提高他们向市场推出创新药物和疗法的能力,从而增强他们的竞争地位。
全球监管事务外包市场的特点是参与者众多,包括老牌企业和新兴组织。 市场上的主要参与者越来越注重与各种利益相关者的伙伴关系和合作,包括非营利会员协会、合同研究组织 (CRO)、技术提供商和生物制药公司。这些合作旨在简化监管流程、增强合规能力并利用先进技术进行高效的数据管理。
通过与非营利协会合作,公司可以获得行业见解和政策倡导,而与 CRO 的合作则可以提供临床试验管理和监管提交方面的专业知识。
最新动态
常见问题