Renseignez-vous maintenant
Marché des tests de compétence en laboratoire
Taille des tests en laboratoire Taille du marché, part, croissance et analyse de l'industrie, par technologie (culture cellulaire, réaction en chaîne en polymérase (PCR), immunoessais, chromatographie, spectrométrie), par l'industrie (diagnostic clinique, pharmaceutique, biologie, microbiologie), par l'utilisateur final (hôpitaux et cliniques, laboratoires académiques et recherche) et analyse régionale,, analyse, analyse, analyse, hôpitaux et cliniques, académique et recherche) et analyse régionale,, analyse,, analyse, analyse, analyse, hôpitaux et cliniques, académique et recherche), et analyse régionale,, Analyse,, Analyse, Analyse,, Analyse,, Hôpitals et cliniques, académique et recherche) et Régiology Analysis, 2025-2032
Pages: 160 | Année de base: 2024 | Version: August 2025 | Auteur: Sunanda G.
Définition du marché
Les tests de compétence en laboratoire sont un processus d'évaluation de la qualité externe qui évalue la capacité d'un laboratoire à générer des résultats de test précis et fiables. Il a comparé les performances avec des normes prédéfinies et des laboratoires de pairs, garantissant le respect des cadres de qualité mondiale tels que l'Organisation internationale pour la normalisation (ISO), les amendements d'amélioration des laboratoires cliniques (CLIA) et le College of American Pathologists (CAP).
Le marché couvre les diagnostics cliniques, les tests de nourriture et de boissons, les produits pharmaceutiques, la surveillance environnementale et les tests de cannabis, où la précision et la fiabilité sont essentielles. Les laboratoires mettent en œuvre des tests de compétence pour l'accréditation, la conformité réglementaire, la détection des erreurs et l'analyse comparative des performances pour maintenir la crédibilité et respecter les normes de l'industrie.
Marché des tests de compétence en laboratoireAperçu
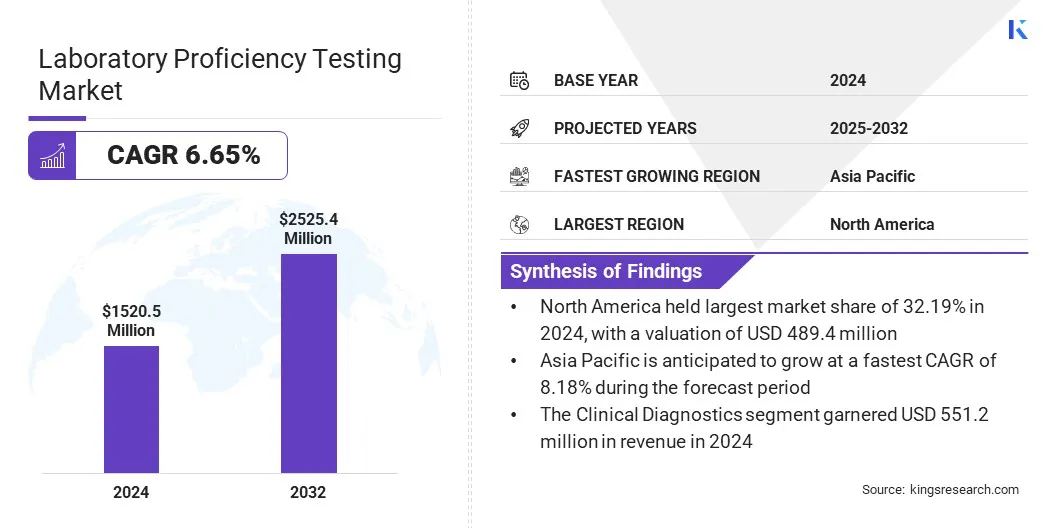
La taille du marché mondial des tests de compétence en laboratoire était évaluée à 1 520,50 millions USD en 2024 et devrait passer de 1 609,49 millions USD en 2025 à 2 525,39 millions USD d'ici 2032, présentant un TCAC de 6,65% au cours de la période de prévision.
La croissance du marché est tirée par les exigences réglementaires et d'accréditation, ce qui a incité les laboratoires à participer à des programmes de PT pour se conformer à des normes telles que CLIA et ISO. De plus, l'intégration de l'automatisation et du Big Data dans les programmes PT rationalise les flux de travail, réduit les erreurs et permet une analyse comparative plus précise entre les laboratoires.
Faits saillants clés
- La taille de l'industrie des tests de compétence en laboratoire était évaluée à 1 520,50 millions USD en 2024.
- Le marché devrait croître à un TCAC de 6,65% de 2025 à 2032.
- L'Amérique du Nord a détenu une part de 32,19% en 2024, évaluée à 489,45 millions USD.
- Le segment de la réaction en chaîne par polymérase (PCR) a récolté 343,94 millions USD de revenus en 2024.
- Le segment des diagnostics cliniques devrait atteindre 891,27 millions USD d'ici 2032.
- Le segment des laboratoires académiques et de recherche a obtenu la plus grande part de revenus de 34,71% en 2024.
- L'Asie-Pacifique devrait croître à un TCAC de 8,18% au cours de la période de prévision.
Les grandes entreprises opérant sur le marché des tests de compétence en laboratoire sont le College of American Pathologists, API, Randox Laboratories Ltd., UK Neqas Microbiology, EMQN, Weqas, SKML, Genqa, LGC Clinical Diagnostics (Seracare), Association of American Feed Control Officiel, AOAC International, CTS, Inc., Instand, Institut de référence pour Bioanalyt, et iqmh.
Le marché connaît une forte croissance avec l'importance croissante de tests de diagnostic précis et fiables. L'adoption accrue de diagnostics moléculaires, de techniques de culture cellulaire et de tests spécialisés met en évidence la nécessité de programmes de test de compétence robustes pour garantir la qualité et la conformité. Le passage à la médecine personnalisée augmente encore la demande, car les laboratoires doivent valider les résultats axés sur la précision pour les applications spécifiques à la maladie.
Des initiatives récentes, telles que le College of American Pathologists (CAP) lançant des régimes de test de compétence spécifiques à H5N1, soulignent comment les programmes sur mesure évoluent pour répondre aux besoins émergents des soins de santé.
- En juin 2025, le College of American Pathologists a lancé le programme de détection et de sous-typage H5N1. Ce programme fournit deux échantillons créés en laboratoire qui simulent des échantillons de patients réalistes, permettant aux laboratoires américains de vérifier leur précision dans la détection et la différenciation de H5N1 des souches de grippe saisonnières.
Moteur du marché
Exigences réglementaires et d'accréditation
Le marché des tests de compétence en laboratoire est alimenté par des exigences strictes réglementaires et d'accréditation qui obligent les laboratoires à participer à des tests de compétence. Des normes telles que les amendements d'amélioration du laboratoire clinique (CLIA) aux États-Unis et ISO / IEC 17025 appliquent la précision, la fiabilité et la conformité de la fiabilité entre les processus de test.
Ces réglementations font des tests de compétence une validation de performance cohérente critique et non facultative. Les secteurs, y compris les soins de santé, les produits pharmaceutiques et la sécurité alimentaire, génèrent une demande de services de test de compétence pour maintenir l'assurance qualité et l'approbation réglementaire.
- En juillet 2024, les Centers for Medicare & Medicaid Services (CMS) ont finalisé les réglementations CLIA, élargissant les exigences de test de compétence pour des analytes supplémentaires et le resserrement des critères de performance. Les analytes nouvellement inclus tels que l'hémoglobine A1C nécessitent désormais des tests de compétence, tandis que les seuils d'erreur admissibles pour des tests tels que l'hématocrite, les globules rouges et les dénombrements de globules blancs ont été réduits jusqu'à 40%.
Défi du marché
Capitaux de capital élevé et opérationnels
Un défi clé entravant les progrès du marché des tests de compétence en laboratoire est l'investissement élevé requis pour les équipements analytiques avancés et les processus de test. Les laboratoires s'appuient sur des technologies telles que la chromatographie liquide-spectrométrie de masse en tandem (LC-MS / MS), qui impliquent une configuration importante et des dépenses opérationnelles.
De plus, les coûts associés à la préparation des échantillons, à la logistique, à la manipulation des données et au recrutement de personnel qualifié créent une pression financière supplémentaire, en particulier pour les petits laboratoires avec des budgets limités.
Pour relever ce défi, les acteurs du marché offrent des systèmes de gestion des données basés sur le cloud, développant des modèles de consortium de partage des coûts et introduisant des solutions de test évolutives qui réduisent les besoins en capital initial. Ces approches facilitent la participation plus large à des programmes de test de compétence tout en facilitant la charge financière des laboratoires liés aux ressources.
Tendance
Adoption croissante de l'automatisation et des mégadonnées dans les programmes PT
Le marché des tests de compétence en laboratoire assiste à une tendance notable vers l'adoption croissante de l'automatisation et de l'intelligence artificielle pour moderniser les processus de test. Les plates-formes automatisées réduisent l'intervention manuelle, minimisant les erreurs dans la gestion des échantillons, la distribution et les rapports.
Les analyses axées sur l'IA permettent une évaluation plus rapide et plus précise de la performance en laboratoire, de découvrir des modèles et des écarts qui peuvent être négligés par évaluation conventionnelle. L'utilisation de Big Data soutient en outre l'analyse comparative dans plusieurs laboratoires, améliorant l'assurance qualité, la conformité et l'efficacité globale des programmes de test de compétence.
- En février 2025, Cormay Diagnostics s'est associé au Scheme d'évaluation de la qualité Randox (RIQAS) pour fournir des programmes d'évaluation de la qualité externe de classe mondiale (EQA). Le partenariat permet l’évaluation des solutions de diagnostic in vitro (IVD) de Cormay Diagnostics au sein du vaste réseau mondial de services EQA de Riqas. La collaboration implique l'application d'outils de rapports numériques et d'analyses dans le processus d'évaluation.
Instantané du rapport sur le marché des tests de compétence en laboratoire
|
Segmentation |
Détails |
|
Par technologie |
Culture cellulaire, réaction en chaîne par polymérase (PCR), immunoessais, chromatographie, spectrométrie, autres |
|
Par industrie |
Diagnostics cliniques, produits pharmaceutiques, biologiques, microbiologie |
|
Par l'utilisateur final |
Hôpitaux et cliniques, laboratoires universitaires et de recherche, organisations de recherche sous contrat (CRO), laboratoires de santé publique |
|
Par région |
Amérique du Nord: États-Unis, Canada, Mexique |
|
Europe: France, Royaume-Uni, Espagne, Allemagne, Italie, Russie, reste de l'Europe | |
|
Asie-Pacifique: Chine, Japon, Inde, Australie, ASEAN, Corée du Sud, reste de l'Asie-Pacifique | |
|
Moyen-Orient et Afrique: Turquie, U.A.E., Arabie saoudite, Afrique du Sud, reste du Moyen-Orient et de l'Afrique | |
|
Amérique du Sud: Brésil, Argentine, reste de l'Amérique du Sud |
Segmentation du marché
- Par technologie (culture cellulaire, réaction en chaîne en polymérase (PCR), immunoessais, chromatographie, spectrométrie et autres): Le segment de réaction en chaîne par polymérase (PCR) a gagné 343,94 millions USD en 2024, principalement en raison de son utilisation généralisée dans les diagnostics moléculaires et les tests de la maladie infectieuse.
- Par industrie (diagnostic clinique, pharmaceutique, biologiques et microbiologie): le segment clinique de diagnostic a détenu une part de 36,25% en 2024, largement attribuée à la large gamme de tests de laboratoire essentiels, qui soutient les hôpitaux, les diagnostics externes pour les travailleurs de la conformité, la conformité et la fiabilité des hôpitaux, des centres de diagnostic et des laboratoires de recherche.
- Par l'utilisateur final (hôpitaux et cliniques, laboratoires académiques et de recherche, organisations de recherche sous contrat (CRO) et laboratoires de santé publique): Le segment des laboratoires académiques et de recherche devrait atteindre 846,43 millions USD d'ici 2032, en raison de volumes élevés de tests complexes, d'adhésion stricte à la recherche de la recherche et à un besoin continu pour une valorisation externe.
Marché des tests de compétence en laboratoireAnalyse régionale
Sur la base de la région, le marché a été classé en Amérique du Nord, en Europe, en Asie-Pacifique, au Moyen-Orient et en Afrique et en Amérique du Sud.
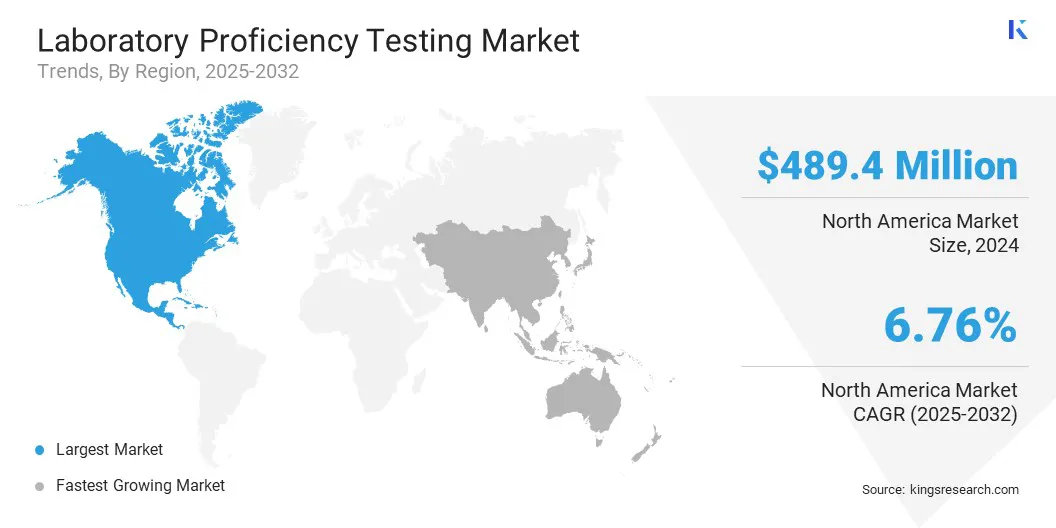
La part de marché des tests de compétence en Laboratory en Amérique du Nord était de 32,19% en 2024, évaluée à 489,45 millions USD. Cette domination est renforcée par la présence de principales sociétés pharmaceutiques et biotechnologiques. L'investissement continu dans la découverte de médicaments, le développement des vaccins et la fabrication de biologiques nécessite des tests de laboratoire fiables.
De plus, la surveillance réglementaire de la US Food and Drug Administration (FDA) incite les laboratoires à adopter des programmes de PT pour respecter la conformité et maintenir la crédibilité dans les essais cliniques et l'assurance qualité.
- En avril 2024, la Food and Drug Administration des États-Unis (FDA) a finalisé une règle classifiant les tests développés en laboratoire (LDT) comme des dispositifs médicaux en vertu de la loi fédérale sur la nourriture, la drogue et la cosmétique. La règle a introduit un élimination de quatre ans du pouvoir discrétionnaire de l'agence, établissant un calendrier de conformité mis en scène pour les laboratoires. L'étape 1 commence en mai 2025 et oblige les laboratoires à se conformer àReprésentation de l'appareil, indication de correction et de suppression et maintenance des fichiers de plainte.
De plus, la région est à la pointe de la médecine de précision et du diagnostic moléculaire, alimenté par une utilisation croissante detests génétiques, panneaux d'oncologie et diagnostics des maladies infectieuses. L'expansion des modèles de traitement personnalisés en Amérique du Nord crée une demande cohérente de fournisseurs de PT, car les laboratoires ont besoin d'une validation externe pour assurer la fiabilité des tests à enjeux élevés.
L'industrie des tests de compétence en laboratoire en Asie-Pacifique devrait croître à un TCAC de 8,18% au cours de la période de prévision. Cette croissance est soutenue par l'expansion des laboratoires de diagnostic dans la région, caractérisés par l'augmentation des dépenses de santé et une base de patients en croissance.
Alors que les laboratoires effectuent des volumes plus élevés de tests dans des domaines tels que les maladies infectieuses et l'oncologie, la participation aux régimes de PT est devenue de plus en plus importante pour maintenir la crédibilité et respecter les normes d'accréditation. La demande de technologies diagnostiques avancées renforce encore la nécessité d'une vérification de qualité cohérente.
- En 2024, Agilus Diagnostics a élargi son réseau de laboratoires et a obtenu des accréditations internationales supplémentaires. La société a prolongé son empreinte à travers l'Inde, le Moyen-Orient et l'Asie du Sud, opérant plus de 418 laboratoires.
De plus, les préoccupations liées à la qualité des aliments et à la contamination ont dirigé les autorités réglementaires en Asie-Pacifique pour renforcer les normes de sécurité, entraînant une plus grande adoption de tests obligatoires dans les laboratoires alimentaires.
Cadres réglementaires
- Aux États-Unis, les modifications d'amélioration du laboratoire clinique (CLIA), codifiées dans le cadre du Code de la réglementation fédérale de la partie 493, obligeant que les laboratoires effectuant des tests de diagnostic humain doivent participer à des programmes de tests de compétence approuvés. Les réglementations spécifient les numéros d'échantillons minimums pour chaque événement de test, y compris cinq spécimens pour la bactériologie, et sont supervisés par les Centers for Medicare & Medicaid Services (CMS). Le non-respect des normes peut entraîner des sanctions, notamment la perte de certification.
- Au Royaume-Uni, l'assurance de la qualité de laboratoire est supervisée par le Royaume-Uni d'accréditation du Royaume-Uni (UKAS), le seul organisme national nommé par le gouvernement. Les laboratoires médicaux doivent se conformer à l'ISO 15189: 2022 - Laboratoires médicaux: exigences en matière de qualité et de compétence, ce qui nécessite une participation à des régimes externes d'assurance qualité, y compris des tests de compétence.
- En Chine, l'assurance de la qualité de laboratoire est régie par la National Health Commission (NHC) et mise en œuvre par le biais du National Center for Clinical Laboratories (NCCL). Les laboratoires cliniques sont tenus de participer à des programmes d'évaluation de la qualité externe nationaux et régionaux, qui sont la forme de test de compétence du pays.
- En Inde, le Conseil national d'accréditation pour les laboratoires de tests et d'étalonnage (NABL), en vertu du Conseil de la qualité de l'Inde (QCI), régit l'accréditation des tests de laboratoire et de compétence. Les laboratoires effectuant des diagnostics médicaux doivent se conformer à l'ISO 15189, tandis que les fournisseurs de PT sont accrédités en vertu de l'ISO / IEC 17043: Évaluation de la conformité - Exigences générales pour les tests de compétence.
- Corée du SudGère l'accréditation du laboratoire par le biais du Korea Laboratory Accreditation Scheme (KOLAS), exploité par l'Agence coréenne pour la technologie et les normes (KATS). Les laboratoires sont accrédités selon les normes internationales, notamment ISO / IEC 17025, ISO 15189 et ISO / IEC 17043, avec une participation obligatoire à des tests de compétence au moins une fois tous les trois ans pour chaque domaine d'accréditation.
Paysage compétitif
Les acteurs du marché de l'industrie des tests de compétence en laboratoire adoptent des stratégies telles que l'élargissement de la portée de leurs programmes de test de compétence, la collaboration avec des sociétés de diagnostic spécialisées et l'intégration des technologies avancées pour améliorer la précision et la couverture des tests, pour maintenir la compétitivité.
Ils investissent également dans la recherche et le développement pour introduire de nouveaux modules de test, améliorant la fiabilité de leurs services dans différentes disciplines de laboratoire. Les partenariats stratégiques et les mises à niveau technologiques aident les fournisseurs à répondre aux besoins émergents de diagnostic et à maintenir la conformité réglementaire.
- En 2024, le Royal College of Pathologists of Australasia Quality Assurance Programs (RCPAQAP) a élargi son programme de diagnostic pédiatrique de 10 à 12 échantillons. Cet ajustement visait à améliorer l'exhaustivité du programme et à soutenir les laboratoires pour évaluer la maîtrise du diagnostic pédiatrique. De plus, RCPAQAP a lancé une étude pilote d'assurance de qualité externe (EQA) pour la détection des mutations dans le cancer du poumon, en collaboration avec Roche.
Les entreprises clés du marché des tests de compétence en laboratoire:
- Le College of American Pathologists
- API
- Randox Laboratories Ltd.
- Microbiologie britannique
- Emqn
- Weqas
- Skml
- Genqa
- Diagnostic clinique LGC (Seracare)
- Association des responsables du contrôle des aliments américains
- AOAC International
- CTS, Inc.
- Installer
- Institut de référence pour les bioanalytiques
- Iqmh
Développements récents (lancement de produit)
- En mars 2023, CAP a lancé un nouveau programme de test de compétence axé sur le virus Monkeypox (MPOX). Cette initiative visait à améliorer l'assurance qualité des processus de test moléculaire et à contribuer à l'assurance de résultats de test précis et fiables, aidant à la détection du virus MPOX.
Questions fréquemment posées
