Jetzt anfragen
Markt für Laborkompetenzen
Laboratory Proficiency Testing Market Size, Share, Growth & Industry Analysis, By Technology (Cell Culture, Polymerase Chain Reaction (PCR), Immunoassays, Chromatography, Spectrometry), By Industry (Clinical Diagnostics, Pharmaceuticals, Biologics, Microbiology), By End User (Hospitals & Clinics, Academic & Research Laboratories), and Regional Analysis, 2025-2032
Seiten: 160 | Basisjahr: 2024 | Veröffentlichung: August 2025 | Autor: Sunanda G.
Marktdefinition
Labor -Kompetenz -Tests sind ein externer Qualitätsbewertungsprozess, der die Fähigkeit eines Labors bewertet, genaue und zuverlässige Testergebnisse zu generieren. Es verglichen die Leistung mit vordefinierten Standards und Peer -Laboratorien und stellte die Einhaltung globaler Qualitätsrahmen wie die internationale Organisation für Standardisierung (ISO), Änderungen der klinischen Laborverbesserung (CLIA) und College of American Pathologists (CAP) sicher.
Der Markt erstreckt sich über klinische Diagnostika, Lebensmittel- und Getränkeprüfungen, Pharmazeutika, Umweltüberwachung und Cannabiskestellen, bei denen Genauigkeit und Zuverlässigkeit von entscheidender Bedeutung sind. Laboratorien implementieren Kompetenztests für Akkreditierung, Vorschriften für die Vorschriften, Fehlererkennung und Leistungsbenchmarking, um die Glaubwürdigkeit aufrechtzuerhalten und die Branchenstandards zu erfüllen.
Markt für LaborkompetenzenÜberblick
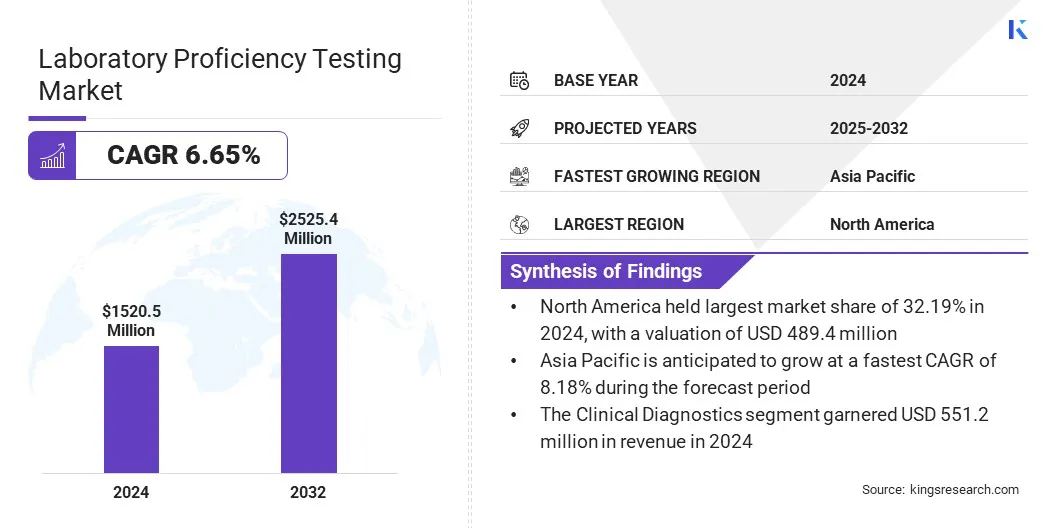
Die Marktgröße für den globalen Laborprofession Testing wurde im Jahr 2024 mit 1.520,50 Mio. USD bewertet und wird voraussichtlich von 1.609,49 Mio. USD im Jahr 2025 auf 2.525,39 Mio. USD bis 2032 wachsen und im Prognosezeitraum einen CAGR von 6,65% aufwiesen.
Das Marktwachstum wird von regulatorischen und akkreditierten Anforderungen angetrieben und die Labors dazu veranlasst, an PT -Programmen teilzunehmen, um Standards wie CLIA und ISO einzuhalten. Darüber hinaus optimiert die Integration von Automatisierung und Big -Data in PT -Programme die Workflows, reduziert Fehler und ermöglicht genauere Benchmarking über Laboratorien hinweg.
Schlüsselhighlights
- Die Größe der Laborprofession Testing der Branche wurde im Jahr 2024 mit 1.520,50 Mio. USD bewertet.
- Der Markt wird voraussichtlich von 2025 bis 2032 mit einer CAGR von 6,65% wachsen.
- Nordamerika hatte im Jahr 2024 einen Anteil von 32,19% im Wert von 489,45 Mio. USD.
- Das PCR -Segment (Polymerase Chain Reaction) erzielte 2024 einen Umsatz von 343,94 Mio. USD.
- Das klinische Diagnostiksegment wird voraussichtlich bis 2032 891,27 Mio. USD erreichen.
- Das Segment Academic & Research Laboratories gewann 2024 den größten Umsatzanteil von 34,71%.
- Der asiatisch -pazifische Raum wird voraussichtlich im Prognosezeitraum auf einer CAGR von 8,18% wachsen.
Große Unternehmen, die auf dem Markt für Laborprodukte testen, sind die College of American Pathologists, API, Randox Laboratories Ltd., UK NEQAS Microbiology, EMQN, WEQAS, SKML, Genqa, LGC Clinical Diagnostics (Seracare), Association of American Feed Control Officers, AOAC International, CTS, Inc., Inc.
Der Markt verzeichnet ein starkes Wachstum mit der steigenden Bedeutung genauer und zuverlässiger diagnostischer Tests. Eine verstärkte Einführung molekularer Diagnostika, Zellkulturmetechniken und spezialisierten Assays unterstreicht die Notwendigkeit robuster Programmen für die Bekenntnis, um Qualität und Einhaltung sicherzustellen. Die Verschiebung in Richtung personalisierter Medizin erhöht die Nachfrage weiter, da die Laboratorien präzisionsgetriebene Ergebnisse für krankheitsspezifische Anwendungen validieren müssen.
Jüngste Initiativen wie das College of American Pathologists (CAP), das H5N1-spezifische Profizidentests-Programme starten, zeigen, wie sich zu maßgeschneiderten Programmen entwickeln, um die anstrengenden Gesundheitsbedürfnisse zu decken.
- Im Juni 2025 startete das College of American Pathologists das H5N1 Influenza A Detection and Subtyping -Programm. Dieses Programm bietet zwei Labor-erstellte Proben, die realistische Patientenproben simulieren, sodass Laboratorien in den USA ihre Genauigkeit bei der Erkennung und Differenzung von H5N1 von saisonalen Grippestämmen überprüfen können.
Marktfahrer
Regulatorische und akkreditierte Anforderungen
Der Markt für Laborkompetenzprüfungen wird durch strenge regulatorische und akkreditierte Anforderungen angeheizt, die Laboratorien für die Teilnahme an Kompetenztests vorschreiben. Standards wie die Änderungen der klinischen Laborverbesserung (CLIA) in den USA und ISO/IEC 17025 erzwingen weltweit die Genauigkeit, Zuverlässigkeit und Einhaltung von Testprozessen.
Diese Vorschriften machen das Testen von Kenntnissen zu einer kritischen, nicht optionalen und unterstützenden konsistenten Leistungsvalidierung. Sektoren wie Gesundheitswesen, Pharmazeutika und Lebensmittelsicherheit erzeugen Nachfrage nach Kompetenzprüfungsdiensten, um die Qualitätssicherung und die behördliche Genehmigung aufrechtzuerhalten.
- Im Juli 2024 haben die Centers for Medicare & Medicaid Services (CMS) die CLIA -Vorschriften abgeschlossen, wodurch die Anforderungen an die Fähigkeitstests für zusätzliche Analyten und die Verschärfung der Leistungskriterien erweitert wurden. Neu enthaltene Analyten wie Hämoglobin A1C erfordern nun Kompetenztests, während zulässige Fehlerschwellen für Tests wie Hämatokrit, rote Blutkörperchen und weiße Blutkörperchenzahlen um bis zu 40%verringert wurden.
Marktherausforderung
Hohe Kapital- und Betriebskosten
Eine zentrale Herausforderung, die den Fortschritt des Marktes für Laborprofessionen behindert, ist die hohe Investition, die für fortschrittliche Analysegeräte und Testprozesse erforderlich ist. Laboratorien stützen sich auf Technologien wie Flüssigchromatographie-Tandem-Massenspektrometrie (LC-MS/MS), die signifikante Einrichtungs- und Betriebsausgaben umfassen.
Darüber hinaus führen die Kosten, die mit der Vorbereitung der Stichproben, der Logistik, der Datenbearbeitung und der Einstellung von Fachpersonal verbunden sind, einen weiteren finanziellen Druck aus, insbesondere für kleinere Labors mit begrenzten Budgets.
Um diese Herausforderung zu befriedigen, bieten Marktteilnehmer Cloud-basierte Datenmanagementsysteme an, entwickeln Kostenteilung Konsortiummodelle und führen skalierbare Testlösungen ein, die den Voraus Kapitalanforderungen reduzieren. Diese Ansätze ermöglichen eine breitere Teilnahme an Programmen für Kompetenzprüfungen und erleichtern die finanzielle Belastung für ressourcenbezogene Labors.
Markttrend
Steigende Einführung von Automatisierung und Big Data in PT -Programmen
Auf dem Markt für Laborprofessionen werden ein bemerkenswerter Trend zur steigenden Einführung von Automatisierung und künstlicher Intelligenz zur Modernisierung von Testprozessen verzeichnet. Automatisierte Plattformen reduzieren die manuelle Intervention und minimieren Fehler bei der Behandlung, Verteilung und Berichterstattung.
AI-gesteuerte Analysen ermöglichen eine schnellere und genauere Bewertung der Laborleistung und entdecken Muster und Abweichungen, die durch konventionelle Bewertung übersehen werden können. Die Verwendung von Big Data unterstützt das Benchmarking in mehreren Labors weiter und verbessert die Qualitätssicherung, Einhaltung und Gesamteffizienz bei Programmen zur Bekanntgabe von Fähigkeiten.
- Im Februar 2025 hat die Cormay Diagnostics mit dem Randox International Quality Assessment Scheme (RIQAS) zusammengearbeitet, um externe Programme für erstklassige Qualitätsbewertungen (EQA) bereitzustellen. Die Partnerschaft ermöglicht die Bewertung der In -vitro -Diagnostischen (IVD) -Lösungen von Cormay Diagnostics im umfangreichen globalen EQA -Services -Netzwerk von RIQAS. Die Zusammenarbeit umfasst die Anwendung digitaler Berichterstattungsinstrumente und -analysen im Bewertungsprozess.
Marktbericht für Laborkompetenzprüfungen Snapshot
|
Segmentierung |
Details |
|
Nach Technologie |
Zellkultur, Polymerasekettenreaktion (PCR), Immunoassays, Chromatographie, Spektrometrie, andere |
|
Nach Industrie |
Klinische Diagnostik, Pharmazeutika, Biologika, Mikrobiologie |
|
Nach Endbenutzer |
Krankenhäuser und Kliniken, akademische und Forschungslabors, Vertragsforschungsorganisationen (CROS), Laboratorien für öffentliche Gesundheit |
|
Nach Region |
Nordamerika: USA, Kanada, Mexiko |
|
Europa: Frankreich, Großbritannien, Spanien, Deutschland, Italien, Russland, Rest Europas | |
|
Asiatisch-pazifik: China, Japan, Indien, Australien, ASEAN, Südkorea, Rest des asiatisch-pazifischen Raums | |
|
Naher Osten und Afrika: Türkei, U.A.E., Saudi -Arabien, Südafrika, Rest von Naher Osten und Afrika | |
|
Südamerika: Brasilien, Argentinien, Rest Südamerikas |
Marktsegmentierung
- Nach Technologie (Zellkultur, Polymerasekettenreaktion (PCR), Immunoassays, Chromatographie, Spektrometrie und anderen): Das Segment Polymerase Chain Reaction (PCR) verdiente sich im Jahr 2024 auf USD 343,94 Millionen, was hauptsächlich auf die breite Verwendung bei molekularen Diagnostik- und Infektionskrankheiten getestet wurde.
- Nach der Industrie (klinische Diagnostik, Pharmazeutika, Biologika und Mikrobiologie): Das Segment der klinischen Diagnostik im Jahr 2024 hatte einen Anteil von 36,25%, das hauptsächlich auf das breite Spektrum der wesentlichen Labortests zugeschrieben wurde, die die Nachfrage nach externen Qualitätsbewertung aufrechterhalten, um die Accuration, die Beschwerde und die Zuverlässigkeit in den Krankenhäusern zu gewährleisten, und Diagnose -Zentren, Diagnose, und Research -Rahmen, und Forschungsvorstellungen.
- Nach Endbenutzern (Krankenhäuser & Kliniken, akademische und Forschungslabors, Vertragsforschungsorganisationen (CROs) und Laboratorien für öffentliche Gesundheit): Das Segment Academic & Research Laboratories wird voraussichtlich 846,43 Mio. USD bis 2032 aufgrund hoher Volumens, strikter Einberufung des Forschungsqualitätsstandards und des Kontinuierstandes für externe Bestätigung erreichen.
Markt für LaborkompetenzenRegionale Analyse
Basierend auf der Region wurde der Markt in Nordamerika, Europa, Asien -Pazifik, Naher Osten und Afrika und Südamerika eingeteilt.
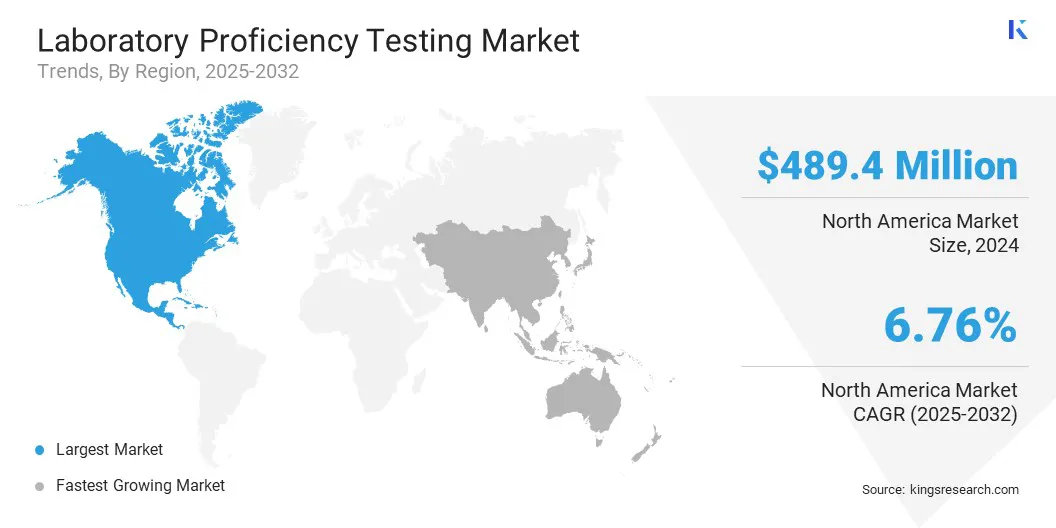
Der Marktanteil von Laboratory Profession Testing North America betrug im Jahr 2024 bei 32,19% im Wert von 489,45 Mio. USD. Diese Dominanz wird durch das Vorhandensein führender pharmazeutischer und biotechnologischer Unternehmen verstärkt. Kontinuierliche Investitionen in die Entdeckung von Arzneimitteln, die Entwicklung von Impfstoffen und die biologische Herstellung erfordern zuverlässige Labortests.
Darüber hinaus veranlasst die regulatorische Aufsicht der US -amerikanischen Food and Drug Administration (FDA) Labors, PT -Programme anzuwenden, um die Compliance zu erfüllen und die Glaubwürdigkeit in klinischen Studien und Qualitätssicherung aufrechtzuerhalten.
- Im April 2024 hat die US-amerikanische Food and Drug Administration (FDA) eine Regel, die labor entwickelte Tests (LDTs) als medizinische Geräte im Rahmen des Bundesgesetzes von Federal Food, Drug und Cosmetic, abgeschlossen hat. In der Regel wurde ein vierjähriges Ausdruck des Ermessensspielraums der Agentur eingeführt, in dem ein festgelegter Zeitplan für Labors festgelegt wurde. Stufe 1 beginnt im Mai 2025 und verlangt von Labors, die medizinische Einhaltung zu erfüllenGeräteberichterstattung, Korrektur- und Entfernungsberichterstattung sowie Wartung von Beschwerdedateien.
Darüber hinaus steht die Region an der Spitze der Präzisionsmedizin und der molekularen Diagnostik, die durch eine wachsende Verwendung von angetrieben wirdGentests, Onkologische Panels und Diagnostik für Infektionskrankheiten. Die Ausweitung personalisierter Behandlungsmodelle in Nordamerika schafft eine konsequente Nachfrage nach PT-Anbietern, da die Laboratorien eine externe Validierung benötigen, um die Zuverlässigkeit bei hohen Einsätzen zu gewährleisten.
Die asiatisch-pazifische Labor-Profizent-Testindustrie wird im Prognosezeitraum auf eine CAGR von 8,18% wachsen. Dieses Wachstum wird durch die Ausdehnung der diagnostischen Labors in der Region unterstützt, die durch steigende Gesundheitsausgaben und eine wachsende Patientenbasis gekennzeichnet ist.
Da Laboratorien höhere Tests von Tests in Bereichen wie Infektionskrankheiten und Onkologie durchführen, ist die Teilnahme an PT -Systemen immer wichtiger geworden, um die Glaubwürdigkeit zu erhalten und die Akkreditierungsstandards zu erfüllen. Die Nachfrage nach fortschrittlichen diagnostischen Technologien verstärkt die Notwendigkeit einer konsistenten Qualitätsprüfung weiter.
- Im Jahr 2024 erweiterte Agilus Diagnostics sein Netzwerk von Labors und erhielt zusätzliche internationale Akkreditierungen. Das Unternehmen erweiterte seinen Fußabdruck in Indien, dem Nahen Osten und Südasien und betrieben über 418 Labors.
Darüber hinaus haben Bedenken im Zusammenhang mit der Qualität und Kontamination von Lebensmitteln die Aufsichtsbehörden im asiatisch -pazifischen Raum dazu veranlasst, die Sicherheitsstandards zu stärken, was zu einer stärkeren Einführung von obligatorischen Tests in Lebensmittellabors führte.
Regulatorische Rahmenbedingungen
- In den USADie Änderungen der klinischen Laborverbesserung (CLIA), die gemäß 42 Code of Federal Regulations Teil 493 kodifiziert wurde, erfordern, dass Laboratorien, die diagnostizierte Tests durch Menschen durchführen, an genehmigten Programmen zur Programmen von zugelassenen Fähigkeiten teilnehmen müssen. In den Vorschriften werden Mindestprobenzahlen für jedes Testereignis angegeben, einschließlich fünf Proben für die Bakteriologie, und werden von den Zentren für Medicare & Medicaid Services (CMS) überwacht. Die Nichteinhaltung von Standards kann zu Sanktionen führen, einschließlich des Verlusts der Zertifizierung.
- In Großbritannien, Laborqualitätssicherung wird vom Vereinigten Königreich Akkreditierungsdienst (UKAs), der von der Regierung ernannten nationalen Körperschaft, überwacht. Medizinische Laboratorien müssen ISO 15189: 2022 - Medizinische Labors: Anforderungen an Qualität und Kompetenz, für die die Teilnahme an externen Qualitätssicherungssystemen, einschließlich Kompetenztests erforderlich ist, erforderlich ist.
- In ChinaDie Laborqualitätssicherung unterliegt der National Health Commission (NHC) und durch das National Center for Clinical Laboratories (NCCL). Klinische Labors sind erforderlich, um an nationalen und regionalen externen Qualitätsbewertungsprogrammen teilzunehmen, die als Form der Fähigkeitstests des Landes dienen.
- In IndienDas National Accreditation Board für Test- und Kalibrierungslabors (NABL) unter dem Quality Council of India (QCI) regelt die Akkreditierung des Labor- und Kompetenztests. Laboratorien, die medizinische Diagnose durchführen, müssen ISO 15189 einhalten, während PT -Anbieter gemäß ISO/IEC 17043: Konformitätsbewertung - allgemeine Anforderungen für Kompetenztests akkreditiert sind.
- SüdkoreaVerwaltet die Laborakkreditierung durch das Korea Laboratory Accreditation Scheme (Kolas), das von der Korean Agency for Technology and Standards (Kats) betrieben wird. Labors werden nach internationalen Standards, einschließlich ISO/IEC 17025, ISO 15189 und ISO/IEC 17043, akkreditiert, wobei mindestens alle drei Jahre für jedes Akkreditierungsfeld mindestens alle drei Jahre beteiligt ist.
Wettbewerbslandschaft
Die Marktteilnehmer in der Labor -Proficance -Testbranche setzen Strategien wie die Erweiterung des Umfangs ihrer Programs für Kompetenzprüfungen, die Zusammenarbeit mit spezialisierten diagnostischen Unternehmen und die Einbeziehung fortschrittlicher Technologien zur Verbesserung der Testgenauigkeit und -versicherung ein, um die Wettbewerbsfähigkeit aufrechtzuerhalten.
Sie investieren auch in Forschung und Entwicklung, um neue Testmodule einzuführen und die Zuverlässigkeit ihrer Dienstleistungen in verschiedenen Labordisziplinen zu verbessern. Strategische Partnerschaften und technologische Upgrades helfen den Anbietern dabei, die aufstrebenden diagnostischen Bedürfnisse zu befriedigen und die Einhaltung der behördlichen Einhaltung aufrechtzuerhalten.
- Im Jahr 2024 erweiterte das Royal College of Pathologists of Australasia Quality Assurance Programs (RCPAQAP) sein pädiatrisches Diagnoseprogramm von 10 auf 12 Proben. Diese Anpassung zielte darauf ab, die Vollständigkeit des Programms zu verbessern und Labors besser zu unterstützen, um die pädiatrische diagnostische Kenntnisse zu bewerten. Darüber hinaus startete RCPAQAP in Zusammenarbeit mit Roche eine Studie zur externen Qualitätssicherung (EQA) zur Erkennung von Mutation bei Lungenkrebs.
Schlüsselunternehmen auf dem Markt für Laborkompetenztests:
- Das College of American Pathologen
- API
- Randox Laboratories Ltd.
- UK NEQAS MICROBIOLOGIE
- Emqn
- Weqas
- Skml
- Genqa
- LGC Clinical Diagnostics (Seracare)
- Vereinigung der amerikanischen Futtermittelkontrollbeamten
- AOAC International
- CTS, Inc.
- Stand
- Referenzinstitut für Bioanalytics
- Iqmh
Jüngste Entwicklungen (Produkteinführung)
- Im März 2023, CAP startete ein neues Programmen für das Professionen, das sich auf das Monkeypox (MPOX) -Virus konzentrierte. Diese Initiative zielte darauf ab, die Qualitätssicherung molekularer Testprozesse zu verbessern und zur Gewissheit präziser und zuverlässiger Testergebnisse beizutragen, was beim Nachweis des MPOX -Virus unterstützt wird.
Häufig gestellte Fragen
