Şimdi Sorun
Laboratuvar Yeterlilik Test Pazarı
Laboratuar Yeterlilik Testleri Pazar Büyüklüğü, Paylaşım, Büyüme ve Endüstri Analizi, Teknoloji (Hücre Kültürü, Polimeraz Zinciri Reaksiyonu (PCR), İmmüno -Alanlar, Kromatografi, Spektrometri), Endüstri (Klinik Teşhis, İlaç, Biyoloji, Mikrobiyoloji), Son Kullanıcı (Hospitals ve Klinikler, Akademik ve Araştırma Laboratuvarları) tarafından 2025-2032
Sayfalar: 160 | Temel Yıl: 2024 | Sürüm: August 2025 | Yazar: Sunanda G.
Pazar tanımı
Laboratuvar yeterlilik testi, bir laboratuvarın doğru ve güvenilir test sonuçları üretme yeteneğini değerlendiren harici bir kalite değerlendirme sürecidir. Önceden tanımlanmış standartlara ve akran laboratuvarlarına göre performansı karşılaştırarak, Uluslararası Standartlar Örgütü (ISO), Klinik Laboratuvar İyileştirme Değişiklikleri (CLIA) ve Amerikan Patologları Koleji (CAP) gibi küresel kalite çerçevelerine uyum sağladı.
Pazar, doğruluk ve güvenilirliğin kritik olduğu klinik teşhis, yiyecek ve içecek testleri, ilaçlar, çevresel izleme ve esrar testlerini kapsamaktadır. Laboratuvarlar, güvenilirliği korumak ve endüstri standartlarını karşılamak için akreditasyon, yasal uyumluluk, hata algılama ve performans kıyaslama için yeterlilik testi uygular.
Laboratuvar Yeterlilik Test PazarıGenel bakış
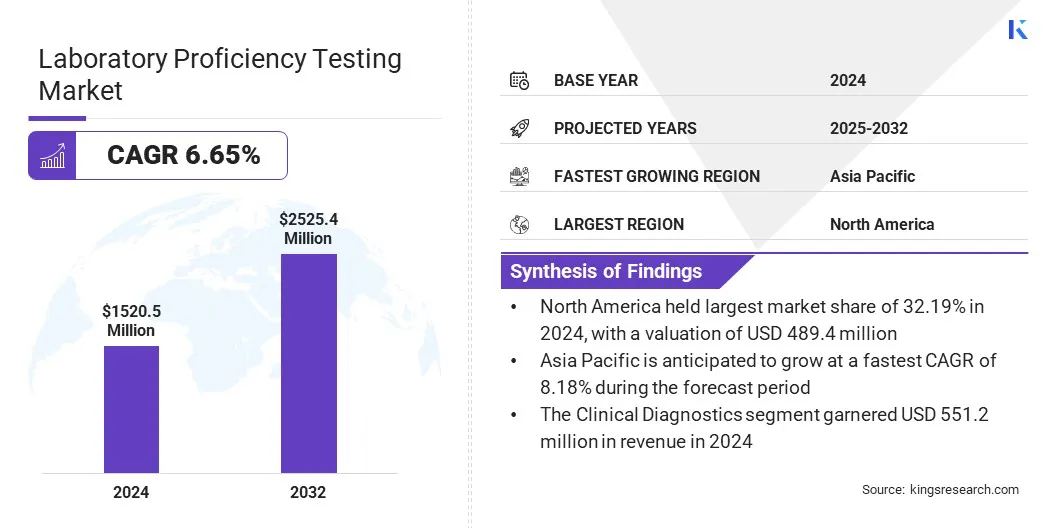
Küresel laboratuvar yeterlilik testi piyasası büyüklüğü 2024'te 1.520.50 milyon ABD Doları değerinde ve 2025'te 1.609.49 milyon ABD Doları'ndan 2032 yılına kadar 2.525.39 milyon USD'ye yükselmesi öngörülüyor.
Pazar büyümesi düzenleyici ve akreditasyon gereksinimleri tarafından yönlendirilir ve laboratuvarların CLIA ve ISO gibi standartlara uyması için PT programlarına katılmalarını istemektedir. Ayrıca, otomasyon ve büyük verilerin PT programlarına entegrasyonu, iş akışlarını kolaylaştırır, hataları azaltır ve laboratuvarlar arasında daha doğru kıyaslama sağlar.
Anahtar önemli noktalar
- Laboratuar yeterlilik testi endüstrisi büyüklüğü 2024'te 1.520.50 milyon ABD Doları değerindeydi.
- Piyasanın 2025'ten 2032'ye kadar% 6,65'lik bir CAGR'de büyümesi bekleniyor.
- Kuzey Amerika, 2024'te 489,45 milyon ABD Doları değerinde% 32.19 oranında bir pay aldı.
- Polimeraz zincir reaksiyonu (PCR) segmenti, 2024 yılında 343,94 milyon ABD Doları gelir elde etti.
- Klinik teşhis segmentinin 2032 yılına kadar 891.27 milyon ABD dolarına ulaşması bekleniyor.
- Akademik ve Araştırma Laboratuvarları segmenti, 2024 yılında% 34,71'lik en büyük gelir payını elde etti.
- Asya Pasifik'in tahmin dönemi boyunca% 8,18'lik bir CAGR'de büyümesi bekleniyor.
Laboratuvar Yeterlilik Test Piyasasında faaliyet gösteren büyük şirketler Amerikan Patologları Koleji, API, Randox Laboratories Ltd., İngiltere NEQAS Mikrobiyolojisi, EMQN, WEQAS, SKML, GenQA, LGC Klinik Teşhisleri (Seracare), Amerikan yem kontrol yetkilileri, Instand, Referans Institute Derneği, AOAC Institute.
Pazar, doğru ve güvenilir teşhis testinin artan önemi ile güçlü bir büyüme yaşıyor. Moleküler teşhislerin, hücre kültürü tekniklerinin ve özel analizlerin artan benimsenmesi, kalite ve uyum sağlamak için sağlam yeterlilik test programlarına duyulan ihtiyacı vurgulamaktadır. Laboratuvarlar hastalığa özgü uygulamalar için hassas odaklı sonuçları doğrulaması gerektiğinden, kişiselleştirilmiş tıbba kayma talebi daha da artırır.
H5N1'e özgü yeterlilik test planlarını başlatan Amerikan Patologlar Koleji (CAP) gibi son girişimler, özel programların gelişmekte olan sağlık ihtiyaçlarını karşılamak için nasıl geliştiğini vurgulamaktadır.
- Haziran 2025'te, Amerikan Patologlar Koleji, H5N1 influenza'yı tespit ve alt tipleme programını başlattı. Bu program, gerçekçi hasta örneklerini simüle eden ve ABD merkezli laboratuvarların H5N1'i mevsimsel grip suşlarından saptama ve farklılaştırma konusundaki doğruluklarını doğrulamasına izin veren iki laboratuvar tarafından oluşturulan örnekler sağlar.
Pazar şoförü
Düzenleyici ve Akreditasyon Gereksinimleri
Laboratuvar yeterlilik test piyasası, laboratuvarları yeterlilik testine katılmaya zorlayan sıkı düzenleyici ve akreditasyon gereksinimleri ile beslenir. Amerika Birleşik Devletleri'nde Klinik Laboratuvar İyileştirme Değişiklikleri (CLIA) ve ISO/IEC 17025 gibi standartlar, test süreçleri arasında küresel olarak doğruluğu, güvenilirliği ve uyumluluğu uygulamaktadır.
Bu düzenlemeler, yeterlilik testini isteğe bağlı değil, tutarlı performans doğrulamasını desteklemektedir. Sağlık hizmetleri, ilaçlar ve gıda güvenliği gibi sektörler, kalite güvencesini ve düzenleyici onayları korumak için yeterlilik test hizmetleri için talep yaratmaktadır.
- Temmuz 2024'te Medicare & Medicaid Hizmetleri Merkezleri (CMS) CLIA düzenlemelerini tamamladı, ek analitler için yeterlilik test gereksinimlerini genişletti ve performans kriterlerini sıkılaştırdı. Hemoglobin A1C gibi yeni dahil edilen analitler artık yeterlilik testi gerektirirken, hematokrit, kırmızı kan hücresi ve beyaz kan hücresi sayıları gibi testler için izin verilen hata eşikleri%40'a kadar azaltılmıştır.
Piyasa Mücadelesi
Yüksek sermaye ve operasyonel maliyetler
Laboratuvar yeterlilik test piyasasının ilerlemesini engelleyen önemli bir zorluk, gelişmiş analitik ekipman ve test süreçleri için gereken yüksek yatırımdır. Laboratuvarlar, önemli kurulum ve operasyonel harcamaları içeren sıvı kromatografisi-tandem kütle spektrometresi (LC-MS/MS) gibi teknolojilere güvenmektedir.
Ayrıca, örnek hazırlama, lojistik, veri işleme ve yetenekli personelin işe alımı ile ilişkili maliyetler, özellikle sınırlı bütçeleri olan daha küçük laboratuvarlar için daha fazla finansal baskı yaratmaktadır.
Bu zorluğu ele almak için pazar oyuncuları bulut tabanlı veri yönetim sistemleri sunuyor, maliyet paylaşımı konsorsiyum modelleri geliştiriyor ve ön sermaye ihtiyaçlarını azaltan ölçeklenebilir test çözümleri sunuyor. Bu yaklaşımlar, kaynak kısıtlı laboratuvarlar üzerindeki mali yükü kolaylaştırırken yeterlilik test programlarına daha geniş katılımı kolaylaştırır.
Pazar trend
PT programlarında otomasyon ve büyük verilerin artan benimsenmesi
Laboratuvar Yeterlilik Test Pazarı, test süreçlerini modernize etmek için otomasyon ve yapay zekanın artmasına yönelik önemli bir eğilime tanık olmaktadır. Otomatik platformlar manuel müdahaleyi azaltır, örnek işleme, dağıtım ve raporlamadaki hataları en aza indirir.
Yapay zeka güdümlü analitikler, laboratuvar performansının daha hızlı ve daha doğru bir şekilde değerlendirilmesini, geleneksel değerlendirme yoluyla göz ardı edilebilecek kalıpları ve sapmaları ortaya çıkarmasını sağlar. Büyük verilerin kullanımı, birden fazla laboratuvarda kıyaslamayı destekler, kalite güvencesini, uyumluluğu ve yeterlilik test programlarında genel verimliliği artırır.
- Şubat 2025'te Cormay Diagnostics, birinci sınıf dış kalite değerlendirme (EQA) programları sağlamak için Randox Uluslararası Kalite Değerlendirme Programı (RIQAS) ile ortaklık kurdu. Ortaklık, Riqas’ın kapsamlı Global EQA Hizmetleri Ağı'ndaki Cormay Diagnostics'in in vitro teşhis (IVD) çözümlerinin değerlendirilmesini sağlar. İşbirliği, değerlendirme sürecinde dijital raporlama araçlarının ve analizlerinin uygulanmasını içerir.
Laboratuvar Yeterlilik Test Pazarı Raporu Anlık Görüntü
|
Segment |
Detaylar |
|
Teknolojiye göre |
Hücre kültürü, polimeraz zincir reaksiyonu (PCR), immüno -tahliller, kromatografi, spektrometri, diğerleri |
|
Sektöre göre |
Klinik teşhis, ilaç, biyolojik, mikrobiyoloji |
|
Son kullanıcı tarafından |
Hastaneler ve Klinikler, Akademik ve Araştırma Laboratuvarları, Sözleşme Araştırma Organizasyonları (CROS), Halk Sağlığı Laboratuvarları |
|
Bölgeye göre |
Kuzey Amerika: ABD, Kanada, Meksika |
|
Avrupa: Fransa, İngiltere, İspanya, Almanya, İtalya, Rusya, Avrupa'nın geri kalanı | |
|
Asya-Pasifik: Çin, Japonya, Hindistan, Avustralya, Asean, Güney Kore, Asya-Pasifik'in Geri Kalanı | |
|
Orta Doğu ve Afrika: Türkiye, U.A.E., Suudi Arabistan, Güney Afrika, Orta Doğu ve Afrika'nın geri kalanı | |
|
Güney Amerika: Brezilya, Arjantin, Güney Amerika'nın geri kalanı |
Pazar segmentasyonu
- Teknoloji (hücre kültürü, polimeraz zincir reaksiyonu (PCR), immüno -tahliller, kromatografi, spektrometri ve diğerleri): polimeraz zincir reaksiyonu (PCR) segmenti, esas olarak moleküler teşhislerde ve bulaşıcı hastalık testlerinde yaygın kullanımı nedeniyle 343.94 milyon USD kazandı.
- Endüstri (klinik teşhis, farmasötikler, biyolojikler ve mikrobiyoloji): Klinik teşhis segmenti, 2024 yılında% 36.25'lik bir pay aldı ve büyük ölçüde hastaneler, tanı merkezleri ve araştırma laboratuvarları arasında hassasiyet, uyarı ve güvenilirlik sağlamak için dış kalite değerlendirmesine olan talebi sürdüren çok çeşitli temel laboratuvar testlerine atfedildi.
- Son kullanıcıya göre (hastaneler ve klinikler, akademik ve araştırma laboratuvarları, sözleşme araştırma organizasyonları (CRO'lar) ve halk sağlığı laboratuvarları): Akademik ve araştırma laboratuvarları segmentinin, yüksek miktarda karmaşık test, araştırma kalitesi standartlarına sıkı sıkıya bağlı kalma ve sürekli ihtiyaç duyulması nedeniyle 2032 yılına kadar 846.43 milyon USD'ye ulaşması öngörülmektedir.
Laboratuvar Yeterlilik Test PazarıBölgesel analiz
Bölgeye dayanarak, pazar Kuzey Amerika, Avrupa, Asya Pasifik, Orta Doğu ve Afrika ve Güney Amerika olarak sınıflandırılmıştır.
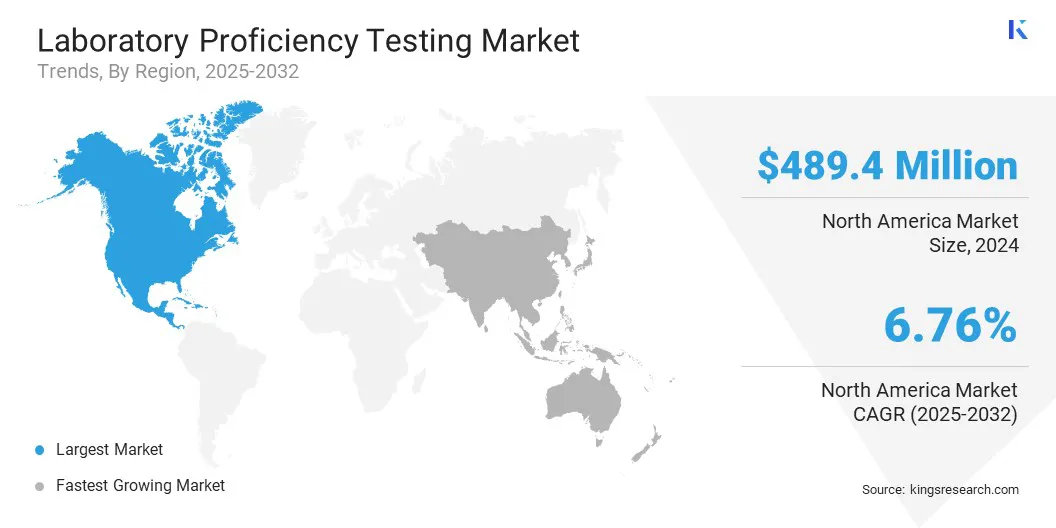
Kuzey Amerika Laboratuvarı Yeterlilik Test pazar payı, 2024'te 489,45 milyon ABD Doları değerinde% 32.19 oranında gerçekleşti. Bu hakimiyet, önde gelen farmasötik ve biyoteknoloji şirketlerinin varlığı ile güçlendirilmiştir. İlaç keşfi, aşı gelişimi ve biyolojik üretimine sürekli yatırım güvenilir laboratuvar testi gerektirir.
Buna ek olarak, ABD Gıda ve İlaç İdaresi'nden (FDA) düzenleyici gözetim, laboratuvarları, klinik çalışmalarda ve kalite güvencesinde uygunluğu karşılamak ve güvenilirliği karşılamak için PT programlarını benimsemeye teşvik eder.
- Nisan 2024'te, ABD Gıda ve İlaç İdaresi (FDA), federal gıda, ilaç ve kozmetik eylemi altında tıbbi cihazlar olarak laboratuvarda geliştirilen testleri (LDTS) sınıflandıran bir kuralı tamamladı. Kural, laboratuvarlar için aşamalı bir uyum zaman çizelgesi oluşturan ajansın icra takdir yetkisinin dört yıllık bir aşamasını getirdi. 1. Aşama Mayıs 2025'te başlar ve laboratuvarların tıbbi olarak uymasını gerektirirCihaz raporlama, düzeltme ve kaldırma raporlaması ve şikayet dosyalarının bakımı.
Dahası, bölge, artan bir kullanımı ile körüklenen hassas tıp ve moleküler teşhislerin ön saflarında yer almaktadır.genetik test, onkoloji panelleri ve bulaşıcı hastalık teşhisi. Kuzey Amerika'daki kişiselleştirilmiş tedavi modellerinin genişletilmesi, laboratuvarların yüksek bahisli testlerde güvenilirliği sağlamak için dış validasyona ihtiyaç duyduğundan, PT sağlayıcıları için tutarlı talep yaratmaktadır.
Asya-Pasifik Laboratuvarı yeterlilik test endüstrisinin tahmin dönemi boyunca% 8,18'lik bir CAGR'de büyüyeceği tahmin edilmektedir. Bu büyüme, artan sağlık harcamaları ve büyüyen bir hasta tabanı ile karakterize edilen bölgedeki teşhis laboratuvarlarının genişlemesi ile desteklenmektedir.
Laboratuvarlar bulaşıcı hastalıklar ve onkoloji gibi alanlarda daha yüksek miktarda test yaptıkça, PT planlarına katılım, güvenilirliği korumak ve akreditasyon standartlarını karşılamak için giderek daha önemli hale gelmiştir. Gelişmiş teşhis teknolojilerine olan talep, tutarlı kalite doğrulama ihtiyacını daha da güçlendirir.
- 2024'te Agilus Diagnostics laboratuvar ağını genişletti ve ek uluslararası akreditasyonlar kazandı. Şirket, 418'den fazla laboratuvar işleterek Hindistan, Orta Doğu ve Güney Asya'da ayak izini uzattı.
Ayrıca, gıda kalitesi ve kontaminasyon ile ilgili endişeler, Asya Pasifik'teki düzenleyici otoritelerin güvenlik standartlarını güçlendirmesine ve gıda laboratuvarlarında zorunlu testlerin daha fazla benimsenmesine neden olmuştur.
Düzenleyici çerçeveler
- ABD'de, 42 Federal Düzenlemeler Kodu 493 uyarınca kodlanan Klinik Laboratuvar İyileştirme Değişiklikleri (CLIA), insan teşhis testi yapan laboratuvarların onaylanmış yeterlilik test programlarına katılması gerektiğini zorunlu kılmaktadır. Düzenlemeler, her test olayı için bakteriyoloji için beş örnek de dahil olmak üzere minimum örnek sayıları belirtir ve Medicare ve Medicaid Hizmetleri Merkezleri (CMS) tarafından denetlenir. Standartların yerine getirilmemesi, sertifika kaybı da dahil olmak üzere yaptırımlara neden olabilir.
- İngiltere'de, laboratuvar kalite güvencesi, hükümet tarafından atanan tek ulusal organ olan Birleşik Krallık Akreditasyon Servisi (UKAS) tarafından denetlenmektedir. Tıbbi laboratuvarlar ISO 15189: 2022 - Tıbbi Laboratuvarlar: Yeterlilik testi de dahil olmak üzere dış kalite güvence planlarına katılmayı gerektiren kalite ve yetkinlik gereksinimleri.
- Çin'de, Laboratuar Kalite Güvencesi Ulusal Sağlık Komisyonu (NHC) tarafından yönetilir ve Ulusal Klinik Laboratuvarlar Merkezi (NCCL) aracılığıyla uygulanır. Klinik laboratuvarların, ülkenin yeterlilik testi biçimi olarak hizmet veren ulusal ve bölgesel dış kalite değerlendirme programlarına katılmaları gerekmektedir.
- Hindistan'da, Hindistan Kalite Konseyi (QCI) uyarınca Test ve Kalibrasyon Laboratuvarları Ulusal Akreditasyon Kurulu (NABL), laboratuvar ve yeterlilik test akreditasyonunu yönetir. Tıbbi teşhis yapan laboratuvarlar ISO 15189'a uygun olmalıdır, PT sağlayıcıları ISO/IEC 17043: Uygunluk Değerlendirmesi - Yeterlilik Testi için Genel Gereksinimler uyarınca akredite edilmiştir.
- Güney KoreKore Teknoloji ve Standartlar Ajansı (Kats) tarafından işletilen Kore Laboratuvarı Akreditasyon Programı (Kolas) aracılığıyla laboratuvar akreditasyonunu yönetir. Laboratuvarlar, ISO/IEC 17025, ISO 15189 ve ISO/IEC 17043 dahil olmak üzere uluslararası standartlar altında akredite edilmiştir ve her bir akreditasyon alanı için en az üç yılda bir yeterlilik testine zorunlu olarak katılır.
Rekabetçi manzara
Laboratuar yeterlilik test endüstrisindeki piyasa oyuncuları, yeterlilik test programlarının kapsamını genişletmek, özel teşhis şirketleriyle işbirliği yapmak ve rekabet gücünü korumak için test doğruluğunu ve kapsamını iyileştirmek için ileri teknolojileri dahil etmek gibi stratejileri benimsemektedir.
Ayrıca, yeni test modülleri tanıtmak için araştırma ve geliştirmeye yatırım yapıyorlar ve hizmetlerinin farklı laboratuvar disiplinlerinde güvenilirliğini artırıyorlar. Stratejik ortaklıklar ve teknolojik yükseltmeler, sağlayıcıların ortaya çıkan teşhis ihtiyaçlarını karşılamalarına ve düzenleyici uyumluluğu sürdürmelerine yardımcı olur.
- 2024 yılında, Avustralasya Kalite Güvence Programları Kraliyet Patologları Koleji (RCPAQAP) pediatrik teşhis programını 10 ila 12 örnek arasında genişletti. Bu ayarlama, programın kapsamlılığını artırmayı ve pediatrik teşhis yeterliliğini değerlendirmede laboratuvarları daha iyi desteklemeyi amaçlamıştır. Ek olarak, RCPAQAP, Roche ile işbirliği içinde akciğer kanserinde mutasyon tespiti için bir Pilot Harici Kalite Güvencesi (EQA) çalışması başlattı.
Laboratuar Yeterlilik Test Piyasasında Kilit Şirketler:
- Amerikalı Patologlar Koleji
- API
- Randox Laboratories Ltd.
- İngiltere Mikrobiyolojisi
- EMQN
- Weqas
- Skml
- Genqa
- LGC Klinik Diyagnostiği (Seracare)
- Amerikan Yem Kontrol Yetkilileri Derneği
- AOAC International
- CTS, Inc.
- İnstand
- Biyoanalitik Referans Enstitüsü
- IQMH
Son gelişmeler (ürün lansmanı)
- Mart 2023'teCAP, Monkeypox (MPOX) virüsüne odaklanan yeni bir yeterlilik test programı başlattı. Bu girişim, moleküler test süreçlerinin kalite güvencesini artırmayı ve MPOX virüsünün tespitine yardımcı olan kesin ve güvenilir test sonuçlarının güvencesine katkıda bulunmayı amaçlamıştır.
Sıkça Sorulan Sorular
