Запросить сейчас
Рынок тестирования лаборатории
Лабораторные тестирование рынка, доля, доля, анализ роста и отрасли, технологии (клеточная культура, полимеразная цепная реакция (ПЦР), иммуноанализа, хроматография, спектрометрия), промышленность (клиническая диагностика, фармацевтические препараты, биологии, микробиология), конечным пользователем (больницы и клиники, академические и исследовательские лаборатории) и региональный анализ, 2025-2032
Страницы: 160 | Базовый год: 2024 | Релиз: August 2025 | Автор: Sunanda G.
Рыночное определение
Тестирование лабораторного мастерства - это процесс оценки внешнего качества, который оценивает способность лаборатории генерировать точные и надежные результаты испытаний. Он сравнил эффективность с предопределенными стандартами и сверстниками лабораторий, обеспечивая соблюдение глобальных структур качества, таких как Международная организация по стандартизации (ISO), клинические поправки по улучшению лаборатории (CLIA) и Колледж американских патологов (CAP).
Рынок охватывает клиническую диагностику, тестирование продуктов питания и напитков, фармацевтические препараты, мониторинг окружающей среды и тестирование каннабиса, где точность и надежность имеют решающее значение. Лаборатории реализуют тестирование на знания по аккредитации, соблюдению нормативных требований, обнаружению ошибок и сравнительным показателям производительности для поддержания доверия и соответствия отраслевым стандартам.
Рынок тестирования лабораторииОбзор
В 2024 году мировой рынок лабораторных испытаний оценивался в 1520,50 млн. Долл. США в 2024 году и, по прогнозам, увеличится с 1 609,49 млн. Долл. США в 2025 году до 2525,39 млн. Долл. США к 2032 году, показав кагр в размере 6,65% в течение прогнозируемого периода.
Рост рынка обусловлен требованиями регулирования и аккредитации, что побуждает лаборатории участвовать в программах PT в соответствии с такими стандартами, как CLIA и ISO. Кроме того, интеграция автоматизации и больших данных в PT -программах упрощает линии рабочих процессов, уменьшает ошибки и позволяет более точный сравнительный анализ в лабораториях.
Ключевые основные моменты
- Размер индустрии тестирования лаборатории оценивался в 1520,50 млн. Долл. США в 2024 году.
- Предполагается, что рынок вырастет в среднем на 6,65% с 2025 по 2032 год.
- В 2024 году Северная Америка владела 32,19% в 2024 году, стоимостью 489,45 миллиона долларов США.
- Сегмент полимеразной цепной реакции (ПЦР) получил 343,94 миллиона долларов США в 2024 году.
- Ожидается, что сегмент клинической диагностики достигнет 891,27 млн. Долл. США к 2032 году.
- Сегмент академических и исследовательских лабораторий обеспечил наибольшую долю дохода в размере 34,71% в 2024 году.
- Ожидается, что в Азиатско -Тихоокеанском регионе вырастет на 8,18% в течение прогнозируемого периода.
Основными компаниями, работающими на рынке тестирования лаборатории, являются Колледж американских патологов, API, Randox Laboratories Ltd., Великобритания Neqas Microbiology, EMQN, WEQAS, SKML, Genqa, LGC Clinical Diagnostics (Seracare), Ассоциация американских чиновников по борьбе с кормами, AOAC International, CTS, Inc., Справочный институт для биоанликов.
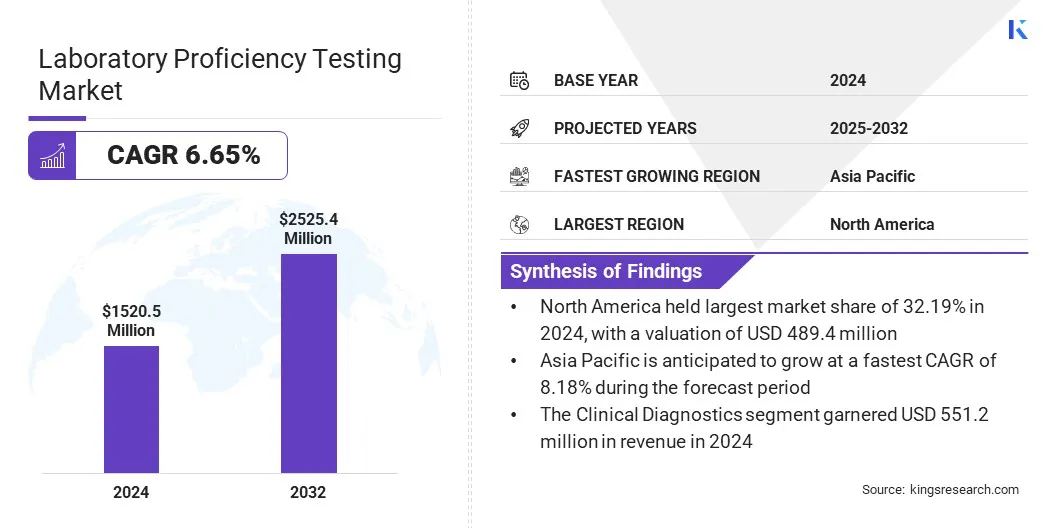
Рынок испытывает сильный рост с растущей важности точного и надежного диагностического тестирования. Повышенное принятие молекулярной диагностики, методов клеточной культуры и специализированных анализов подчеркивает необходимость в надежных программах тестирования квалификации для обеспечения качества и соответствия. Сдвиг в сторону персонализированной медицины еще больше увеличивает спрос, поскольку лаборатории должны подтвердить результаты, основанные на точности для применения для специфичных для заболеваний.
Недавние инициативы, такие как Колледж американских патологов (CAP), запускающий H5N1-специфические схемы тестирования на уклонении, подчеркивают, как разработанные программы развиваются для удовлетворения возникающих потребностей в здравоохранении.
- В июне 2025 года Колледж американских патологов запустил программу H5N1 гриппа A Detection и Subtyping. Эта программа содержит два образца, созданных в лаборатории, которые имитируют реалистичные образцы пациентов, что позволяет лабораториям в США проверить их точность в обнаружении и дифференцировании H5N1 от штаммов сезонного гриппа.
Рыночный драйвер
Требования к регулированию и аккредитации
Рынок тестирования лабораторных знаний подпитывается строгими требованиями регулирования и аккредитации, которые обязывают лаборатории участвовать в тестировании на устойчивость. Такие стандарты, как поправки к улучшению клинической лаборатории (CLIA) в Соединенных Штатах и ISO/IEC 17025 во всем мире, обеспечивают точность, надежность и соблюдение требований в процессах тестирования.
Эти нормы делают квалификацию тестирования критической, а не дополнительной, поддерживающей постоянную проверку эффективности. Секторы, включая здравоохранение, фармацевтические препараты и безопасность пищевых продуктов, вызывают спрос на услуги по тестированию квалификации для поддержания обеспечения качества и одобрения регулирующих органов.
- В июле 2024 года Центры Medicare & Medicaid Services (CMS) завершили правила CLIA, расширив требования к тестированию квалификации для дополнительных аналитов и ужесточание критериев эффективности. Вновь включали аналиты, такие как гемоглобин A1C, теперь требуют тестирования квалификации, в то время как допустимые пороги ошибок для таких тестов, как гематокрит, эритроциты и количество лейкоцитов, были снижены до 40%.
Рыночный вызов
Высокие капитальные и эксплуатационные расходы
Ключевой проблемой, препятствующей прогрессу рынка тестирования лаборатории, являются высокие инвестиции, необходимые для передового аналитического оборудования и процессов тестирования. Лаборатории полагаются на такие технологии, как жидкая хроматография-тандемная масс-спектрометрия (LC-MS/MS), которая включает в себя значительные настройки и эксплуатационные расходы.
Кроме того, затраты, связанные с подготовкой выборки, логистикой, обработкой данных и набором квалифицированного персонала, создают дальнейшее финансовое давление, особенно для небольших лабораторий с ограниченными бюджетами.
Чтобы решить эту проблему, игроки рынка предлагают облачные системы управления данными, разрабатывают модели консорциума распределения затрат и внедряют масштабируемые решения для тестирования, которые снижают потребности в капитале. Эти подходы способствуют более широкому участию в программах тестирования квалификации, одновременно облегчая финансовую нагрузку на лаборатории с ограниченными ресурсами.
Тенденция рынка
Растущее внедрение автоматизации и больших данных в программах PT
Рынок тестирования лабораторных знаний является свидетелем заметной тенденции к растущему внедрению автоматизации и искусственного интеллекта для модернизации процессов тестирования. Автоматизированные платформы уменьшают ручное вмешательство, сводя к минимуму ошибки в обработке образцов, распределении и отчетности.
Аналитика, управляемая ИИ, обеспечивает более быструю и более точную оценку лабораторной эффективности, раскрывая закономерности и отклонения, которые можно упускать из виду посредством обычной оценки. Использование больших данных дополнительно поддерживает сравнительный анализ в нескольких лабораториях, повышение обеспечения качества, соблюдение требований и общую эффективность программ тестирования квалификации.
- В феврале 2025 года Cormay Diagnostics вступила в партнерские отношения с Международной схемой оценки качества Randox (RIQAS) для предоставления программ внешнего оценки качества мирового класса (EQA). Партнерство позволяет оценить решения Cormay Diagnostics 'in vitro Diagnostic (IVD) в обширной глобальной сети услуг EQA Riqas. Сотрудничество включает в себя применение инструментов и аналитики цифровой отчетности в процессе оценки.
Снимок отчета о рынке тестирования лаборатории.
|
Сегментация |
Подробности |
|
По технологиям |
Клеточная культура, полимеразная цепная реакция (ПЦР), иммуноанализа, хроматография, спектрометрия, другие |
|
По промышленности |
Клиническая диагностика, фармацевтические препараты, биологии, микробиология |
|
От конечного пользователя |
Больницы и клиники, академические и исследовательские лаборатории, контрактные исследовательские организации (CRO), лаборатории общественного здравоохранения |
|
По региону |
Северная Америка: США, Канада, Мексика |
|
Европа: Франция, Великобритания, Испания, Германия, Италия, Россия, остальная часть Европы | |
|
Азиатско-Тихоокеанский регион: Китай, Япония, Индия, Австралия, АСЕАН, Южная Корея, остальная часть Азиатско-Тихоокеанского региона | |
|
Ближний Восток и Африка: Турция, США, Саудовская Аравия, Южная Африка, остальная часть Ближнего Востока и Африки | |
|
Южная Америка: Бразилия, Аргентина, остальная часть Южной Америки |
Сегментация рынка
- Технология (клеточная культура, полимеразная цепная реакция (ПЦР), иммуноанализа, хроматография, спектрометрия и другие): сегмент полимеразной цепной реакции (ПЦР) заработал 343,94 млн. Долл. США в 2024 году, в основном из -за его широко распространенного использования при молекулярной диагностике и тестировании инфекционных заболеваний.
- По промышленности (клиническая диагностика, фармацевтические препараты, биологическая и микробиология): в 2024 году сегмент клинической диагностики в размере 36,25%, в значительной степени связанный с широким спектром основных лабораторных испытаний, которые поддерживают спрос на оценку внешнего качества для обеспечения точности, соблюдения и надежности в больницах, диагностических центрах и исследовательских лабораториях.
- Благодаря конечным пользователю (больницы и клиники, академические и исследовательские лаборатории, контрактные исследовательские организации (CRO) и лаборатории общественного здравоохранения): сегмент академических и исследовательских лабораторий, по прогнозам, достигнет 846,43 млн. Долл. США из -за 2032 из -за высоких объемов сложного тестирования, строгого поддержания к стандартам качества исследования и постоянной потребности во внешней валидации.
Рынок тестирования лабораторииРегиональный анализ
Основываясь на регионе, рынок был классифицирован в Северной Америке, Европе, Азиатско -Тихоокеанском регионе, Ближнем Востоке и Африке и Южной Америке.
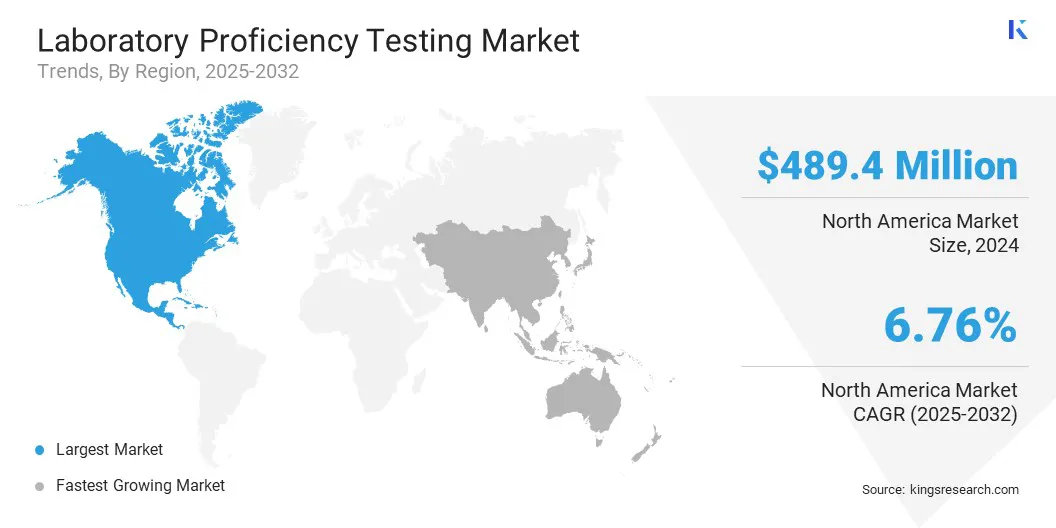
В 2024 году доля рынка тестирования лаборатории в Северной Америке составила 32,19% в 2024 году, стоимостью 489,45 млн. Долл. США. Это доминирование подкрепляется присутствием ведущих фармацевтических и биотехнологических компаний. Непрерывные инвестиции в обнаружение лекарств, развитие вакцин и производство биологических данных требуют надежных лабораторных испытаний.
Кроме того, регулирующий надзор со стороны Управления по контролю за продуктами и лекарствами США (FDA) побуждает лаборатории принять программы PT для соответствия соответствию и поддержанию доверия в клинических испытаниях и обеспечении качества.
- В апреле 2024 года Управление по контролю за продуктами и лекарствами США (FDA) завершило правило, классифицирующее лабораторные тесты (LDT) как медицинские приборы в соответствии с федеральным Законом о продуктах питания, наркотиках и косметическом. Правило ввело четырехлетнее поэтапное обеспечение по усмотрению агентства, установив поэтапный график соответствия для лабораторий. Этап 1 начинается в мае 2025 года и требует, чтобы лаборатории выполняли медицинские услугиОтчеты об отчетности, исправлении и удалении, а также обслуживание файлов жалоб.
Более того, область находится на переднем крае точной медицины и молекулярной диагностики, подпитывая растущим использованиемГенетическое тестирование, онкологические панели и диагностика инфекционных заболеваний. Расширение персонализированных моделей лечения в Северной Америке создает постоянный спрос на поставщиков PT, поскольку лабораториям нуждается в внешней валидации, чтобы обеспечить надежность в испытаниях с высокими ставками.
По оценкам, азиатско-тихоокеанская лабораторная промышленность расти в среднем на 8,18% в течение прогнозируемого периода. Этот рост подтверждается расширением диагностических лабораторий в регионе, характеризующихся растущими расходами на здравоохранение и растущей базой пациентов.
Поскольку лаборатории проводят более высокие объемы тестов в таких областях, как инфекционные заболевания и онкология, участие в схемах PT становится все более важным для поддержания доверия и соответствия стандартам аккредитации. Спрос на передовые технологии диагностики еще больше усиливает необходимость последовательной проверки качества.
- В 2024 году диагностика Agilus расширила свою сеть лабораторий и заработала дополнительные международные аккредитации. Компания расширила свое присутствие по всей Индии, Ближнем Востоке и Южной Азии, работая более чем 418 лабораторий.
Кроме того, опасения, связанные с качеством пищи и загрязнением, привели к тому, что регулирующие органы в Азиатско -Тихоокеанском регионе укрепили стандарты безопасности, что привело к большему принятию обязательных испытаний в пищевых лабораториях.
Нормативные рамки
- В США, Поправки по улучшению клинической лаборатории (CLIA), кодифицированные в соответствии с 42 Кодексом федеральных правил, часть 493, мандат, что лаборатории, проводящие диагностические тестирование человека, должны участвовать в утвержденных программах тестирования. Правила указывают минимальные числа выборки для каждого события тестирования, включая пять образцов для бактериологии, и контролируются центрами услуг Medicare & Medicaid (CMS). Неспособность соответствовать стандартам может привести к санкциям, включая потерю сертификации.
- В Великобритании, Лабораторное обеспечение качества контролируется Службой аккредитации Великобритании (UKAS), единственным национальным органом, назначенным правительством. Медицинские лаборатории должны соблюдать ISO 15189: 2022 - Медицинские лаборатории: требования к качеству и компетентности, которые требуют участия в схемах обеспечения внешнего качества, включая тестирование на владение.
- В Китае, лабораторное обеспечение качества регулируется Национальной комиссией здравоохранения (NHC) и осуществляется через Национальный центр клинических лабораторий (NCCL). Клинические лаборатории обязаны участвовать в национальных и региональных программах оценки внешнего качества, которые служат в качестве формы тестирования в стране.
- В ИндииНациональный совет по аккредитации по тестированию и калибровке лабораторий (NABL) в соответствии с Качественным Советом Индии (QCI) регулирует аккредитацию лаборатории и испытания владения. Лаборатории, выполняющие медицинскую диагностику, должны соблюдать ISO 15189, в то время как поставщики PT аккредитованы в соответствии с ISO/IEC 17043: Оценка соответствия - общие требования для тестирования квалификации.
- Южная КореяУправляет лабораторной аккредитацией по схеме аккредитации Корейской лаборатории (KOLAS), управляемой Корейским агентством по технологиям и стандартам (KATS). Лаборатории аккредитованы по международным стандартам, включая ISO/IEC 17025, ISO 15189 и ISO/IEC 17043, с обязательным участием в тестировании квалификации, по крайней мере, один раз в три года для каждой области аккредитации.
Конкурентная ландшафт
Игроки рынка в индустрии тестирования лаборатории внедряют такие стратегии, как расширение масштабов их программ тестирования, сотрудничества со специализированными диагностическими компаниями и включение передовых технологий для повышения точности и охвата тестирования, для поддержания конкурентоспособности.
Они также инвестируют в исследования и разработки, чтобы ввести новые модули тестирования, повышая надежность их услуг в различных лабораторных дисциплинах. Стратегические партнерские отношения и технологические обновления помогают поставщикам удовлетворять возникающие диагностические потребности и поддерживать соответствие нормативным требованиям.
- В 2024 году Королевский колледж патологов программ по обеспечению качества Австралии (RCPAQAP) расширил свою программу диагностики педиатрической диагностики с 10 до 12 образцов. Эта корректировка была направлена на повышение полноценной программы и лучшую поддержку лабораторий в оценке у детей диагностики. Кроме того, RCPAQAP запустил исследование Pilot External Assure Calizer (EQA) для обнаружения мутаций при раке легких, в сотрудничестве с Roche.
Ключевые компании на рынке тестирования лаборатории:
- Колледж американских патологов
- API
- Randox Laboratories Ltd.
- Великобритания Neqas Microbiology
- Emqn
- Weqas
- SKML
- Genqa
- LGC Клиническая диагностика (Seracare)
- Ассоциация американских чиновников по контролю за кормом
- AOAC International
- Cts, Inc.
- Инстанд
- Справочный институт биоаналитики
- IQMH
Последние разработки (запуск продукта)
- В марте 2023 года, CAP выпустила новую программу тестирования на упругость, ориентированная на вирус MonkeyPox (MPOX). Эта инициатива была направлена на повышение обеспечения качества процессов молекулярного тестирования и способствовать обеспечению точных и надежных результатов теста, помогая в обнаружении вируса MPOX.
Часто задаваемые вопросы
