薬事アウトソーシング市場
薬事アウトソーシング市場規模、シェア、成長および業界分析、サービス別(規制コンサルティング、法的代理、提出準備と管理、品質とコンプライアンス、その他)、アプリケーション別、エンドユーザー別(製薬会社およびバイオテクノロジー会社、医療機器メーカー)、および地域分析、 2024-2031
ページ: 190 | 基準年: 2023 | リリース: 2025年1月 | 著者: Sunanda G. | 最終更新: 2026年3月
今すぐお問い合わせ
ページ: 190 | 基準年: 2023 | リリース: 2025年1月 | 著者: Sunanda G. | 最終更新: 2026年3月
規制関連業務のアウトソーシングとは、一般に製薬、バイオテクノロジー、医療機器、ヘルスケアなどの業界で、規制遵守タスクをサードパーティのサービスプロバイダーに委託する行為を指します。
このアプローチには、規制戦略の開発、文書の準備、製品承認のための申請の提出、コンプライアンスの監視、および市販後の調査の管理が含まれます。これにより、組織は、多様な世界市場にわたるコンプライアンスを効率的に確保しながら、研究開発などの中核的な活動に集中することができます。
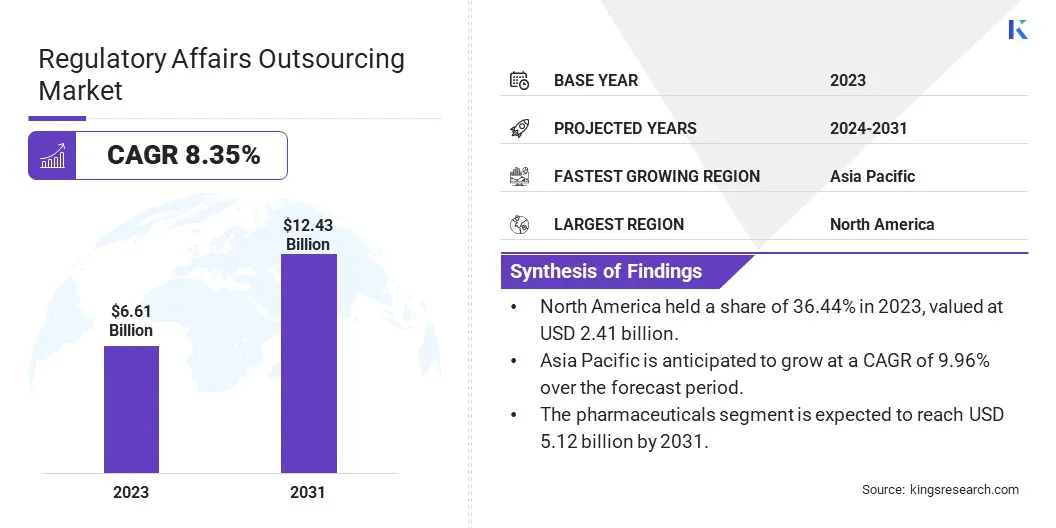
世界の規制業務アウトソーシング市場規模は、2023年に66億1,000万米ドルと評価され、2024年の70億9,000万米ドルから2031年までに124億3,000万米ドルに成長すると予測されており、予測期間中に8.35%のCAGRを示します。
市場は、世界的な規制枠組みの複雑さの増大と、費用対効果の高いコンプライアンス ソリューションに対する需要の高まりにより、大幅な成長を遂げています。さらに、臨床試験の拡大、先進的治療薬の台頭、市販後調査への注目の高まりが市場拡大をさらに加速させています。
世界の薬事アウトソーシング市場で活動している主要企業は、Accell Clinical Research, LLC、Genpact、WuXi AppTec、Medpace、Charles River Laboratories、CRITERIUM, INC.、iuvo BioScience, llc.、Covance、Freyr、ICON plc、PHARMALEX GMBH.、Groupe ProductLife S.A.、Parexel International (MA) Corporation、Biomapas Group、Thermo Fisher Scientific Inc. です。 (PPD)など。
規制関連業務のアウトソーシングは、品質とコンプライアンスへの重点を高めることに貢献し、市場の成長を促進します。規制機関は、特に医療や製薬などの規制の厳しい業界において、安全性と品質基準をますます重視しています。
市場の推進力
「世界中で臨床試験の数が増加」
世界中で臨床試験の数が増加しているため、薬事アウトソーシング市場の成長が加速しています。イノベーションと新しい治療法の開発への注目が高まるにつれ、世界中で実施される臨床試験の数が増加しています。
承認の取得、現地の規制への準拠の確認、必要な文書の提出など、これらの治験の規制面の管理は複雑で時間がかかります。
アウトソーシング パートナーは、世界的な規制要件に関する専門知識を備えており、承認プロセスを合理化し、遅延を軽減し、必要な規制基準に従って臨床試験が確実に実施されるように支援します。臨床試験における規制上のサポートに対する需要の増加により、市場の拡大がさらに促進されます。
市場の課題
「複数の地域での規制遵守への取り組み」
規制業務アウトソーシング市場の成長を抑制する重要な要因は、複数の地域にわたって異なる規制要件へのコンプライアンスを維持するという課題です。世界市場では規制、文書化基準、承認スケジュールに大きな違いが見られ、アウトソーシングされたサービスプロバイダーにとって複雑さが生じています。
この変動により、遅延、エラー、コンプライアンス違反の可能性のリスクが高まり、アウトソーシングされた業務の効率と有効性に影響を与えます。
この課題に対処するために、企業はますます高度なデジタル ツールを導入し、人工知能 (AI)規制プロセスを合理化し、文書の正確性を確保します。 AI を活用したプラットフォームを活用することで、プロバイダーはリアルタイムの更新と予測分析を提供することで、変化する規制に適応できます。
さらに、企業は規制状況をより効果的に対処するために、現地チームを設立したり、市場の専門家と提携したりすることで、地域固有の専門知識に投資しています。これらのアプローチにより、適応性が強化され、コンプライアンスのリスクが最小限に抑えられ、サービス提供が改善され、市場の成長に対する規制の複雑さの影響が軽減されます。
市場動向
「デジタルヘルスのトレンドにより規制上のアウトソーシングが増加」
モバイルヘルスアプリ、ウェアラブル、遠隔医療ソリューションなどのデジタルヘルス製品とサービスの急速な拡大は、規制業務アウトソーシング市場の成長に貢献しています。規制当局は、デジタルヘルスイノベーションによってもたらされる特有の課題に対処するための新しいフレームワークを開発しています。
これらの製品では、多くの場合、データプライバシーの問題、サイバーセキュリティ基準、新しい臨床試験要件など、規制遵守に対して異なるアプローチが必要となります。
デジタルヘルスソリューションを開発している企業は、進化する規制に対処するために、この分野の専門知識を持つアウトソーシング会社に頼るようになっています。
| セグメンテーション | 詳細 |
| サービス別 | 規制コンサルティング、法的代理、提出準備と管理、品質とコンプライアンス、その他 |
| 用途別 | 医薬品、医療機器、生物製剤、その他 |
| エンドユーザー別 | 製薬およびバイオテクノロジー企業、医療機器メーカー、受託研究機関 (CRO) |
| 地域別 | 北米:アメリカ、カナダ、メキシコ |
| ヨーロッパ:フランス、イギリス、スペイン、ドイツ、イタリア、ロシア、その他のヨーロッパ | |
| アジア太平洋:中国、日本、インド、オーストラリア、ASEAN、韓国、その他のアジア太平洋地域 | |
| 中東とアフリカ:トルコ、UAE、サウジアラビア、南アフリカ、その他の中東およびアフリカ | |
| 南アメリカ:ブラジル、アルゼンチン、その他の南米諸国 |
地域に基づいて、世界市場は北米、ヨーロッパ、アジア太平洋、中東およびアフリカ、ラテンアメリカに分類されています。

北米の規制業務アウトソーシング市場は、2023 年に約 36.44% という注目すべきシェアを占め、その価値は 24 億 1,000 万米ドルに達しました。この地域の確立された製薬産業とバイオテクノロジー産業がこの拡大を推進しています。医薬品の承認件数が増加し、臨床試験、治療薬の継続的な革新には、複雑な承認プロセスをナビゲートする専門の規制サービスが必要です。
企業が製品開発スケジュールを加速しながら、FDA などの厳しい規制要件を満たすことを目指しているため、専門的な規制業務のアウトソーシングに対する需要が高まっています。
アジア太平洋地域は、予測期間中に 9.96% という最速の CAGR で成長すると予測されています。アジア太平洋地域の製薬およびバイオテクノロジー部門は、研究開発投資の増加、バイオ医薬品の進歩、ヘルスケア市場の拡大によって急速な成長を遂げています。
この地域ではバイオテクノロジー企業や製薬企業の数が増加しており、規制に関する専門知識に対する需要が高まっています。
規制業務をアウトソーシングすることで、これらの企業は国内および国際的な規制の複雑さを管理できるようになり、革新的な医薬品や治療法を市場に導入する能力が向上し、それによって競争力が強化されます。
世界の規制業務アウトソーシング市場は、既存の企業と新興組織の両方を含む多数の参加者によって特徴付けられます。 市場の主要企業は、非営利会員協会、受託研究機関 (CRO)、テクノロジープロバイダー、バイオ医薬品企業など、さまざまなステークホルダーとのパートナーシップやコラボレーションにますます重点を置いています。これらのコラボレーションは、規制プロセスを合理化し、コンプライアンス機能を強化し、高度なテクノロジーを活用して効率的なデータ管理を行うことを目的としています。
非営利団体と連携することで、企業は業界の洞察や政策擁護にアクセスできる一方、CRO とのパートナーシップにより臨床試験管理や規制当局への申請に関する専門知識を得ることができます。
最近の動向
よくある質問