治験管理システム市場
臨床試験管理システム市場規模、シェア、成長および業界分析、コンポーネント別(ソフトウェア、サービス)、配信モード別(Webおよびクラウドベース、オンプレミス)、エンドユーザー別(製薬会社および生物製薬会社、医療機器会社、その他)および地域分析、 2025-2032
ページ: 170 | 基準年: 2024 | リリース: July 2025 | 著者: Versha V. | 最終更新: November 2025
今すぐお問い合わせ
治験管理システム市場
ページ: 170 | 基準年: 2024 | リリース: July 2025 | 著者: Versha V. | 最終更新: November 2025
臨床試験管理システム (CTMS) は、規制要件へのコンプライアンスを確保しながら、臨床試験の計画、実行、監視を容易にするように設計された特殊なソフトウェア プラットフォームです。
この市場には、臨床試験の計画、予算編成、施設管理、被験者の追跡、報告をサポートするソフトウェアとサービスが含まれます。これには、製薬会社、受託研究機関、学術機関が採用するクラウドベースおよびオンプレミスのプラットフォームが含まれます。
このレポートは、予測期間中に市場の発展に影響を与えると予想される地域分析と規制枠組みに裏付けられた主要な成長ドライバーの概要を示しています。
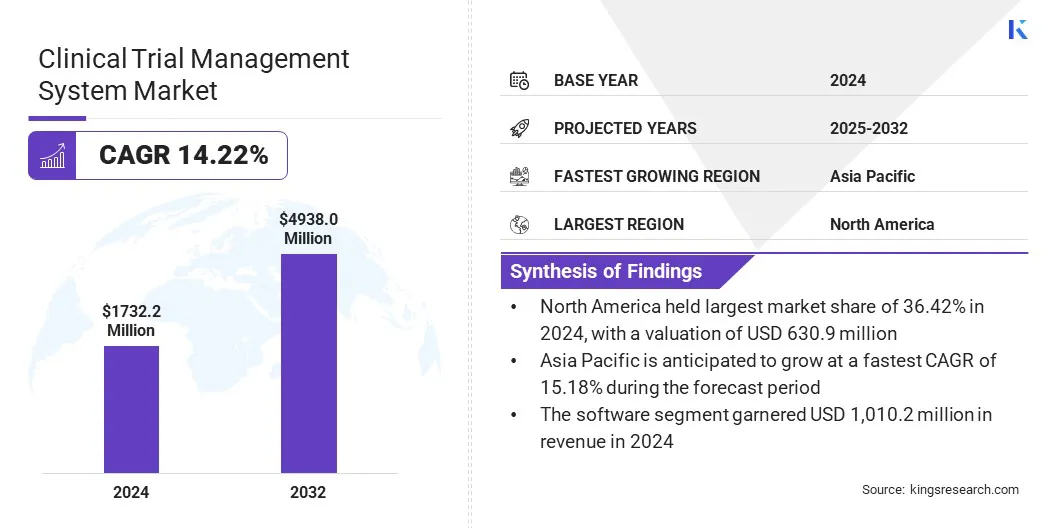
Kings Research によると、世界の臨床試験管理システム市場規模は 2024 年に 17 億 3,220 万米ドルと評価され、2025 年の 19 億 4,650 万米ドルから 2032 年までに 49 億 3,800 万米ドルに成長すると予測されており、予測期間中に 14.22% の CAGR を示しています。
この市場は、臨床試験の数の増加と試験プロトコルの複雑さの増大により、着実な成長を遂げています。製薬会社やバイオテクノロジー会社による治験業務の合理化と法規制順守の確保を目的としたデジタルプラットフォームの採用の増加は、市場の拡大に大きく貢献しています。
臨床試験管理システム業界で活動する主要企業は、Oracle、IQVIA、Veeva Systems Inc.、Dassault Systèmes、RealTime Software Solutions, LLC、CIOCoverage、PHARMASEAL、Wipro、Castor、Salesforce, Inc.、Advarra、Cloudbyz、Fortrea、SimpleTrials、および Clario です。
分散型治験への移行とリアルタイム データ アクセスのニーズの高まりにより、クラウドベースの CTMS ソリューションの採用が促進されています。これらのプラットフォームは、柔軟性、拡張性、分散した研究サイト間でのコラボレーションの向上を提供し、進化する試験モデルとうまく連携します。
クラウドベースの CTMS ソリューションの使用は、データ管理の改善、より高速なワークフローの実現、分散型試験運用のサポートによって市場の成長に貢献しています。
リアルタイムのデータ アクセスと効果的なサイト管理のニーズの高まりにより、市場は着実に成長しています。臨床試験の複雑さの増大と世界的な拡大により、効率的な監視を優先する必要性が高まっています。
スポンサーや受託研究組織は、業務効率を高め、法規制順守を確保するために、患者登録、施設の生産性、プロトコル順守、有害事象報告などの主要業績評価指標をリアルタイムで可視化することを求めています。運用データおよび臨床データへのリアルタイム アクセスにより、より迅速な意思決定がサポートされ、遅延が軽減され、研究全体の実行が向上します。
この開発は、リアルタイム データ アクセスとサイト調整の合理化に対する需要の高まりに対応しています。これは、CTMS プラットフォームの採用を促進する、データ主導型の試験運用と効率的な実行への継続的な移行を反映しています。
臨床試験管理システム市場における主な課題は、研究受託機関 (CRO)、スポンサー、治験施設間の技術プラットフォームの断片化です。この断片化により、データの切断、ワークフローの一貫性の欠如、コミュニケーションの障壁が生じ、コラボレーションが妨げられ、試験活動が遅延します。
異なるソフトウェア システム間の相互運用性の欠如は、冗長なタスク、管理コストの増加、サプライ チェーン管理の課題につながります。これらの非効率性は、スケジュール、データ品質、規制遵守に悪影響を及ぼします。
これに対処するために、ベンダーは、複数のサードパーティ プラットフォームとのシームレスな統合を可能にする、ベンダーに依存しない CTMS ソリューションを採用しています。この統合により、一元的なデータ管理と統一されたワークフローが促進され、自動化されたサプライ チェーン プロセスですべての関係者が調整されるため、治験の効率が向上し、運用リスクが軽減されます。
CTMS 市場の主要なトレンドは、臨床試験ソリューションと高度なデータ プラットフォームおよび人工知能 (AI) テクノロジーの統合です。この統合により、複数のソースからの広範な臨床データのシームレスな集約、分析、管理が可能になり、データの精度とアクセスしやすさが向上します。 AI を活用したツールにより、予測分析、リスク評価、およびワークフローの自動化これにより、患者の募集、モニタリング、全体的な治験の効率が向上します。
|
セグメンテーション |
詳細 |
|
コンポーネント別 |
ソフトウェア、サービス |
|
配信モード別 |
Web およびクラウドベース、オンプレミス |
|
エンドユーザー別 |
製薬会社、バイオ医薬品会社、医療機器会社、その他 |
|
地域別 |
北米:アメリカ、カナダ、メキシコ |
|
ヨーロッパ: フランス、イギリス、スペイン、ドイツ、イタリア、ロシア、その他のヨーロッパ | |
|
アジア太平洋地域: 中国、日本、インド、オーストラリア、ASEAN、韓国、その他のアジア太平洋地域 | |
|
中東とアフリカ: トルコ、アラブ首長国連邦、サウジアラビア、南アフリカ、その他の中東およびアフリカ | |
|
南アメリカ: ブラジル、アルゼンチン、その他の南米 |
地域に基づいて、市場は北米、ヨーロッパ、アジア太平洋、中東およびアフリカ、南米に分類されています。
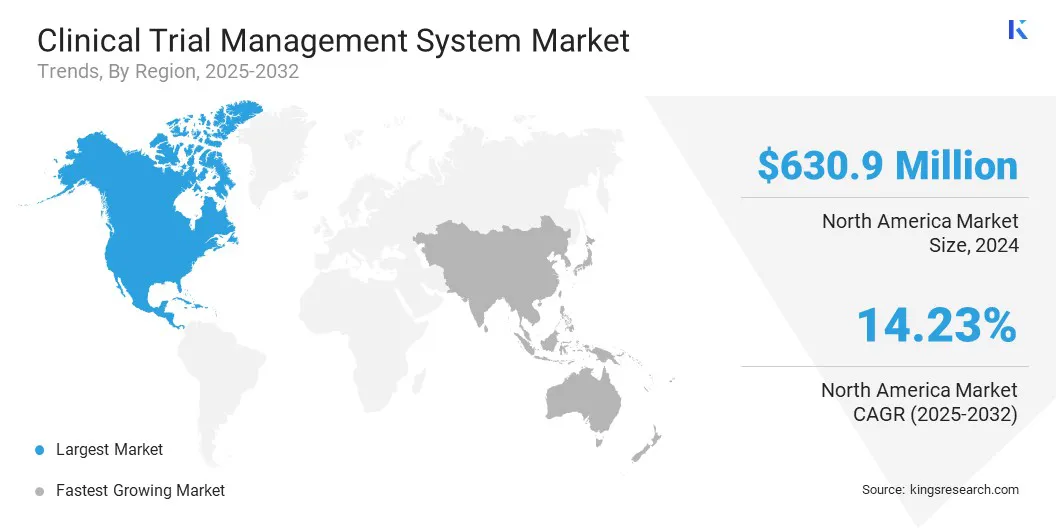
北米は2024年の臨床試験管理システム市場の36.42%のシェアを占め、評価額は6億3,090万米ドルとなった。この地域の優位性は、進行中の大量の臨床試験に起因しています。たとえば、世界保健機関のデータによると、米国では 7,008 件の臨床試験が登録されています。
これは、治験業務を効率化するために先進的なデジタルプラットフォームを積極的に導入している大手製薬会社や受託研究機関の強力な存在によってさらに支えられています。さらに、臨床開発に携わる学術医療センターや研究大学の存在も、堅牢な治験管理システムに対する安定した需要に貢献しています。
アジア太平洋地域の臨床試験管理システム業界は、市場で最も急速な成長を記録すると予想されており、予測期間中のCAGRは15.18%と予測されています。この成長は、試験運用と調整を改善するためのデジタル システムの使用の増加によって支えられています。
たとえば、オーストラリアでは、ニューサウスウェールズ州の健康すべての公衆衛生機関に集中臨床試験管理システムを導入しました。このプラットフォームは、財務管理、参加者の追跡、予測、レポート作成を合理化するための共有オンライン環境として機能し、それによって地域での臨床試験実施の効率を高めます。
さらに、この地域における多国籍製薬会社の存在感の増大により、堅牢な CTMS インフラストラクチャの必要性が加速しています。
これらの企業は、コスト効率の向上、迅速な患者募集、多様な人々へのアクセスの恩恵を受けるために、第 II 相および第 III 相臨床試験をアジア太平洋地域にアウトソーシングするケースが増えています。これにより、地域の規制基準と運用の複雑さを満たしたスケーラブルな CTMS ソリューションに対する強い需要が生まれています。
臨床試験管理システム市場は、継続的な技術の進歩、プラットフォームの統合、参加者間の戦略的統合によって特徴付けられています。主要企業は、複雑な治験ワークフローをサポートするモジュール式の相互運用可能なプラットフォームの開発を通じて、ソリューション機能の拡張に注力しています。
この発表は、特にスタートアップ段階における運用の非効率性に対処する、統合されたエンドツーエンドのソリューションの提供に向けたベンダー間の広範な戦略的転換を反映しています。
さらに、分散型およびハイブリッド試用モデルをサポートするために、企業はクラウドネイティブ アーキテクチャとリアルタイム分析への投資を増やしています。これらの戦略は、機能、統合の深さ、運用効率によって定義される競争環境を形成しています。
最近の開発 (製品の発売)
よくある質問